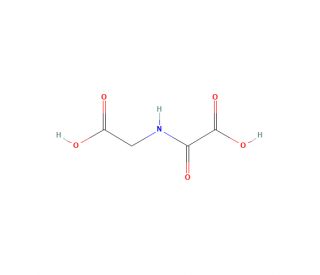
N-Oxalylglycine (CAS 5262-39-5)
Ver las publicaciones del producto (5)
ENLACES RÁPIDOS
La N-Oxalilglicina es un compuesto que funciona como inhibidor competitivo de las dioxigenasas dependientes de 2-oxoglutarato. Actúa quelando el hierro del sitio activo, impidiendo así la unión del cosustrato e inhibiendo la actividad enzimática. El mecanismo de acción de la N-Oxalilglicina consiste en interrumpir el ciclo catalítico de las dioxigenasas dependientes de 2-oxoglutarato, que intervienen en diversos procesos biológicos como la desmetilación del ADN y de las histonas, así como en las vías de respuesta a la hipoxia. Al interferir con la actividad enzimática de estas dioxigenasas, la N-Oxalilglicina puede utilizarse para investigar las funciones específicas de estas enzimas en procesos celulares y vías de señalización. Su capacidad para inhibir competitivamente el hierro del sitio activo puede ser útil para estudiar los mecanismos moleculares subyacentes a las funciones de las dioxigenasas dependientes de 2-oxoglutarato en diversas aplicaciones experimentales.
N-Oxalylglycine (CAS 5262-39-5) Referencias
- Cinética y espectroscópicos de investigación de CoII, NiII, y N-oxalylglycine la inhibición de la FeII/alfa-cetoglutarato dioxigenasa, TauD. | Kalliri, E., et al. 2005. Biochem Biophys Res Commun. 338: 191-7. PMID: 16165092
- Síntesis y actividad de la N-oxalilglicina y sus derivados como inhibidores de la histona lisina desmetilasa con dominio C de Jumonji. | Hamada, S., et al. 2009. Bioorg Med Chem Lett. 19: 2852-5. PMID: 19359167
- Un nuevo antagonista etiladenina de los receptores de adenosina A(2A): caracterización conductual y bioquímica como fármaco antiparkinsoniano. | Volke, M., et al. 2009. PLoS One. 4: e7875. PMID: 19924283
- Diseño de campos de fuerza y simulaciones de dinámica molecular del factor inhibidor HIF-1 y su complejo con inhibidores conocidos: implicaciones para el diseño racional de inhibidores. | Park, H., et al. 2010. J Mol Graph Model. 29: 221-8. PMID: 20663694
- El inhibidor de amplio espectro de la 2-oxoglutarato oxigenasa N-oxalilglicina está presente en las hojas de ruibarbo y espinacas. | Al-Qahtani, K., et al. 2015. Phytochemistry. 117: 456-461. PMID: 26196940
- Novedosa estrategia electroquímica libre de etiquetas para la determinación sensible de la proteína 1 de translocación diez-once. | Yu, Z., et al. 2021. Anal Chim Acta. 1146: 140-145. PMID: 33461709
- Una nueva serie de inhibidores putativos de la histona desmetilasa de Brugia malayi como posibles fármacos antifiláricos. | Kreiss, T., et al. 2022. PLoS Negl Trop Dis. 16: e0010216. PMID: 35294431
- Conservación del inusual pliegue dimérico JmjC de JMJD7 de Drosophila melanogaster a los humanos. | Chowdhury, R., et al. 2022. Sci Rep. 12: 6065. PMID: 35410347
- Corrección editorial: Análogos de MOG para explorar el farmacóforo de MCT2, la biología del α-cetoglutarato y los efectos celulares de la N-oxalilglicina. | Fets, L., et al. 2022. Commun Biol. 5: 1019. PMID: 36167803
- Análisis estructural del sitio de unión del 2-oxoglutarato de la oxigenasa JMJD5 ligada al ritmo circadiano. | Islam, MS., et al. 2022. Sci Rep. 12: 20680. PMID: 36450832
- Un cribado de efectores de alto rendimiento identifica un nuevo andamiaje de moléculas pequeñas para la inhibición de la dioxigenasa 2 de translocación diez-once. | Palei, S., et al. 2022. RSC Med Chem. 13: 1540-1548. PMID: 36545435
- El formaldehído reacciona con los residuos N-terminales de prolina para dar aminales bicíclicos. | John, T., et al. 2023. Commun Chem. 6: 12. PMID: 36698022
- Selectividad de sustrato e inhibición de las hidroxilasas de histidina JmjC MINA53 y NO66. | Türkmen, VA., et al. 2023. RSC Chem Biol. 4: 235-243. PMID: 36908702
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
N-Oxalylglycine, 10 mg | sc-202720 | 10 mg | $53.00 | |||
N-Oxalylglycine, 100 mg | sc-202720A | 100 mg | $153.00 |
