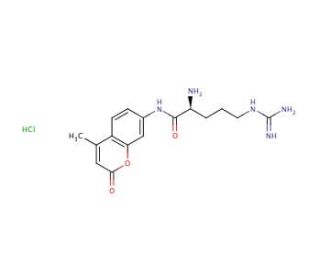
L-Arginine-7-amido-4-methylcoumarin hydrochloride (CAS 69304-16-1)
ACCÈS RAPIDE AUX LIENS
Le chlorhydrate de L-arginine-7-amido-4-méthylcoumarine (LAMCH) est un composé synthétique utilisé en recherche scientifique comme substrat de la cathepsine H. Dérivé de l'acide aminé naturel L-arginine, le chlorhydrate de L-arginine-7-amido-4-méthylcoumarine a trouvé des applications dans diverses expériences de laboratoire impliquant la biochimie, la physiologie et la pharmacologie. Dans la recherche scientifique, le chlorhydrate de L-arginine-7-amido-4-méthylcoumarine a été utilisé dans de multiples contextes. En tant que sonde fluorescente, il permet l'examen de la structure et de la fonction des protéines, ainsi que l'étude des interactions des protéines avec d'autres molécules. Il est utile pour étudier la liaison des ligands aux récepteurs et pour explorer la cinétique des réactions catalysées par les enzymes. En outre, le chlorhydrate de L-arginine-7-amido-4-méthylcoumarine facilite l'examen des effets des médicaments sur diverses voies biochimiques. Bien que le mécanisme d'action précis du chlorhydrate de L-arginine-7-amido-4-méthylcoumarine reste incomplètement compris, on pense qu'il fonctionne en se liant à des récepteurs spécifiques à la surface des cellules, déclenchant une cascade de signalisation qui conduit à divers effets physiologiques et biochimiques. Les effets spécifiques du chlorhydrate de L-arginine-7-amido-4-méthylcoumarine dépendent de la nature de l'expérience menée. En général, il a démontré son influence sur de nombreuses voies biochimiques impliquées dans la signalisation cellulaire, l'expression des gènes, le métabolisme et la prolifération cellulaire. En outre, il peut agir sur des processus physiologiques tels que la pression sanguine, le rythme cardiaque et la respiration.
L-Arginine-7-amido-4-methylcoumarin hydrochloride (CAS 69304-16-1) Références
- Purification et caractérisation d'une arginine aminopeptidase de Lactobacillus sakei. | Sanz, Y. and Toldrá, F. 2002. Appl Environ Microbiol. 68: 1980-7. PMID: 11916721
- Surexpression de peptidases chez Lactococcus et évaluation de leur libération à partir de cellules qui fuient. | Tuler, TR., et al. 2002. J Dairy Sci. 85: 2438-50. PMID: 12416795
- Activité antibactérienne et protéolytique du venin de la guêpe endoparasite Pimpla hypochondriaca (Hymenoptera: Ichneumonidae). | Dani, MP., et al. 2003. J Insect Physiol. 49: 945-54. PMID: 14511827
- Purification et caractérisation fonctionnelle de la rhiminopeptidase A, une nouvelle aminopeptidase du venin de Bitis gabonica rhinoceros. | Vaiyapuri, S., et al. 2010. PLoS Negl Trop Dis. 4: e796. PMID: 20706583
- L'exercice physique et un régime riche en leucine modulent le métabolisme des protéines musculaires chez les rats porteurs de tumeurs de Walker. | Salomão, EM., et al. 2010. Nutr Cancer. 62: 1095-104. PMID: 21058197
- Effet de la sélection pour le taux de croissance sur le vieillissement des myofibrilles, les propriétés de texture de la viande et le potentiel protéolytique du muscle m. longissimus chez le lapin. | Gil, M., et al. 2006. Meat Sci. 72: 121-9. PMID: 22061382
- Outils alimentaires pour moduler le stockage du glycogène dans le muscle de la daurade royale: supplémentation en glycérol. | Silva, TS., et al. 2012. J Agric Food Chem. 60: 10613-24. PMID: 22994592
- Activités protéolytiques dans les filets d'une sélection d'espèces de poissons australiens sous-utilisés. | Ahmed, Z., et al. 2013. Food Chem. 140: 238-44. PMID: 23578639
- Changements dans l'activité de la cathepsine pendant le stockage à basse température et le traitement sous vide de la poitrine de bœuf. | Kaur, L., et al. 2020. Food Sci Anim Resour. 40: 415-425. PMID: 32426720
- Séparation d'une nouvelle alpha-N-benzoylarginine-bêta-naphthylamide hydrolase de la cathepsine B1. Purification, caractérisation et propriétés des deux enzymes du poumon de lapin. | Singh, H. and Kalnitsky, G. 1978. J Biol Chem. 253: 4319-26. PMID: 659418
- Tests fluorimétriques pour la cathepsine B et la cathepsine H avec des substrats de méthylcoumarylamide. | Barrett, AJ. 1980. Biochem J. 187: 909-12. PMID: 6897924
- La cathepsine B, la cathepsine H et la cathepsine L. | Barrett, AJ. and Kirschke, H. 1981. Methods Enzymol. 80 Pt C: 535-61. PMID: 7043200
- Altération de la croissance du virus de la grippe à cycle multiple dans les cellules Vero (OMS) par la perte de l'activité de la trypsine. | Kaverin, NV. and Webster, RG. 1995. J Virol. 69: 2700-3. PMID: 7884927
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
L-Arginine-7-amido-4-methylcoumarin hydrochloride, 5 mg | sc-215211 | 5 mg | $107.00 | |||
L-Arginine-7-amido-4-methylcoumarin hydrochloride, 25 mg | sc-215211A | 25 mg | $233.00 |
