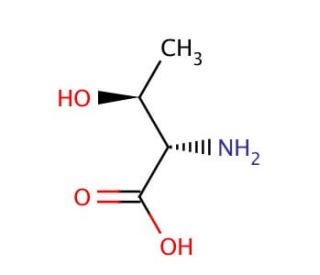
L-allo-Threonine (CAS 28954-12-3)
ENLACES RÁPIDOS
La L-allo-treonina es un isómero del aminoácido treonina, que se distingue por la disposición de sus componentes moleculares, lo que le confiere propiedades únicas que se han convertido en un punto de interés en la investigación bioquímica y de biología estructural. A diferencia de su homóloga, la L-treonina, que se incorpora a las proteínas durante la traducción, la L-allo-treonina no se encuentra en las proteínas, por lo que sirve como herramienta para sondear la estructura, función y estabilidad de las proteínas. Los investigadores aprovechan la L-allo-treonina en el estudio de la especificidad enzimática, explorando cómo las enzimas distinguen entre sustratos estrechamente relacionados. Este isómero también desempeña un papel fundamental en la biología sintética, donde se utiliza para diseñar nuevas proteínas con secuencias de aminoácidos alteradas, lo que permite investigar los mecanismos de plegamiento de las proteínas y diseñar proteínas con nuevas funciones. Además, las propiedades estructurales únicas de la L-allo-treonina la convierten en un componente valioso en el desarrollo de peptidomiméticos, moléculas que imitan la estructura de los péptidos y se utilizan para dilucidar las interacciones a nivel molecular, ofreciendo conocimientos sobre los principios fundamentales del reconocimiento y la unión moleculares.
L-allo-Threonine (CAS 28954-12-3) Referencias
- Estructuras de rayos X de complejos de treonina aldolasa: base estructural del reconocimiento de sustratos. | Kielkopf, CL. and Burley, SK. 2002. Biochemistry. 41: 11711-20. PMID: 12269813
- Caracterización de homólogos de deshidrogenasa/reductasa de cadena corta de Escherichia coli (YdfG) y Saccharomyces cerevisiae (YMR226C). | Fujisawa, H., et al. 2003. Biochim Biophys Acta. 1645: 89-94. PMID: 12535615
- Hacia la síntesis asimétrica preparativa de beta-hidroxi-alfa-aminoácidos: Formación de L-allo-treonina a partir de glicina y acetaldehído utilizando GlyA recombinante. | Makart, S., et al. 2007. J Biotechnol. 130: 402-10. PMID: 17597243
- Evaluación del metabolismo de la treonina in vivo mediante cromatografía de gases/espectrometría de masas e infusión de isótopos estables. | Ballèvre, O., et al. 1991. Anal Biochem. 193: 212-9. PMID: 1908193
- Descubrimiento y caracterización de la D-fenilserina deaminasa de Arthrobacter sp. TKS1. | Muramatsu, H., et al. 2011. Appl Microbiol Biotechnol. 90: 159-72. PMID: 21190106
- Alivio de los síntomas relacionados con el asma mediante un derivado de la L-allo treonina. | Heo, JC. and Lee, SH. 2013. Int J Mol Med. 31: 881-7. PMID: 23381610
- Arg-265: un residuo crítico de la SHMT citosólica de L.donovani en el mantenimiento de la unión del THF y la catálisis. | Gandhi, S., et al. 2015. Exp Parasitol. 149: 16-23. PMID: 25499510
- El importante papel del grupo hidroxilo en la adaptabilidad conformacional del bis(l-treoninato)cobre(II) en comparación con el bis(l-allo-treoninato)cobre(II): Estudio de Química Cuántica. | Marković, M., et al. 2016. Inorg Chem. 55: 7694-708. PMID: 27442350
- Efecto del Nuevo Compuesto LX519290, un Derivado de la L-allo Treonina, sobre el Potencial Antioxidante in Vitro e in Vivo. | Chun, K., et al. 2016. Int J Mol Sci. 17: PMID: 27598126
- La L-treonina y su análogo añadidos al medio sólido autoclavado suprimen la producción de tricoteceno por Fusarium graminearum. | Maeda, K., et al. 2017. Arch Microbiol. 199: 945-952. PMID: 28357472
- Biosíntesis de la Cicloclorotina: Identificación de los Genes Implicados en las Transformaciones Oxidativas y en la O,N-Transacilación Intramolecular. | Jiang, Y., et al. 2021. Org Lett. 23: 2616-2620. PMID: 33736433
- Estudio de Espectroscopia de Terahercios de los Estereoisómeros de la Treonina. | Zeng, R., et al. 2022. Appl Spectrosc. 76: 1132-1141. PMID: 35469427
- Interacciones entre iones cobre (II) y L-treonina, L-allo-treonina y L-serina en solución acuosa. | Grenouillet, P., et al. 1973. Biochim Biophys Acta. 322: 185-94. PMID: 4765086
- Globomicina, un nuevo antibiótico peptídico con actividad formadora de esferoplastos. III. Determinación estructural de la globomicina. | Nakajima, M., et al. 1978. J Antibiot (Tokyo). 31: 426-32. PMID: 670085
- Clonación genética, caracterización bioquímica y función fisiológica de una L-treonina aldolasa termoestable de baja especificidad de Escherichia coli. | Liu, JQ., et al. 1998. Eur J Biochem. 255: 220-6. PMID: 9692922
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
L-allo-Threonine, 250 mg | sc-255235 | 250 mg | $281.00 |
