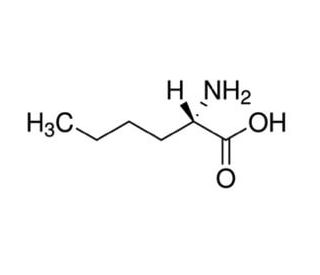
L-(+)-Norleucine (CAS 327-57-1)
ACCÈS RAPIDE AUX LIENS
La L-(+)-Norleucine est un acide aminé non protéinogène qui fonctionne comme un analogue structurel de la leucine. Il peut être utilisé pour étudier les effets des substitutions d'acides aminés sur la structure et la fonction des protéines. La L-(+)-Norleucine peut être incorporée dans des peptides et des protéines au cours de la synthèse chimique afin d'étudier l'impact de la modification de la composition en acides aminés sur l'activité biologique. Son mécanisme d'action implique une interaction avec la machinerie cellulaire responsable de la synthèse des protéines, influençant potentiellement le repliement, la stabilité et l'activité des molécules résultantes. Sa présence dans les systèmes expérimentaux permet d'étudier les effets des modifications des acides aminés sur le comportement et les propriétés des protéines, contribuant ainsi à la compréhension des relations structure-fonction dans les molécules biologiques.
L-(+)-Norleucine (CAS 327-57-1) Références
- Complexes ternaires de cis-(NH(3))(2)PtCl(2) (cis-DDP) avec la guanosine (guo), la cytidine (cyd) et les aminoacides Glycine (gly), L-Alanine (ala), L-2-Aminobutyric Acid (2-aba), L-Norvaline (nval) et L-Norleucine (nleu). | Katsarou, E., et al. 1997. Met Based Drugs. 4: 57-63. PMID: 18475769
- La L-leucine 5-hydroxylase de Nostoc punctiforme est un nouveau type de dioxygénase dépendante du Fe(II)/α-cétoglutarate qui est utile en tant que biocatalyseur. | Hibi, M., et al. 2013. Appl Microbiol Biotechnol. 97: 2467-72. PMID: 22584432
- Dégradation de la lysine chez Candida. Caractérisation et rôle probable des L-norleucine-leucine, 4-aminobutyrate et delta-aminovalerate:2-oxoglutarate aminotransférases. | Der Garabedian, PA. and Vermeersch, JJ. 1989. Biochimie. 71: 497-503. PMID: 2503054
- Structure cristalline de la forme mutante Cys115His de la méthionine γ-lyase de Citrobacter freundii complexée avec de la l-norleucine. | Revtovich, SV., et al. 2017. Biochim Biophys Acta Proteins Proteom. 1865: 1123-1128. PMID: 28602917
- α-amination formelle biocatalytique énantiosélective de l'acide hexanoïque en l-norleucine. | Dennig, A., et al. 2018. Org Biomol Chem. 16: 8030-8033. PMID: 30334043
- Identification de l'incommensurabilité dans la L-leucine: les instabilités de réseau peuvent-elles être considérées comme des phénomènes généraux dans les acides aminés hydrophobes ? | Guinet, Y., et al. 2022. Phys Chem Chem Phys. 24: 27023-27030. PMID: 35946565
- Candida L-norleucine,leucine:2-oxoglutarate aminotransférase. Purification et propriétés. | Der Garabedian, PA. and Vermeersch, JJ. 1987. Eur J Biochem. 167: 141-7. PMID: 3622507
- Sur le rôle des acides aminés à chaîne ramifiée dans le renouvellement des protéines du muscle squelettique. Études in vivo avec la L-norleucine. | Schott, KJ., et al. 1985. Z Naturforsch C Biosci. 40: 427-37. PMID: 3895764
- Études 1H NMR des réactions d'échange d'hydrogène de substrat catalysées par la L-méthionine gamma-lyase. | Esaki, N., et al. 1985. Biochemistry. 24: 3857-62. PMID: 4052371
- La libération d'insuline induite par la leucine et la norleucine dépend-elle de l'activité de l'aminoacide aminotransférase ? | Sener, A., et al. 1983. J Biol Chem. 258: 6693-4. PMID: 6343380
- Inhibition par la L-valine et la L-norleucine de la libération d'insuline induite par le 3-phénylpyruvate. | Sener, A. and Malaisse, WJ. 1984. Biochimie. 66: 353-60. PMID: 6380597
- La [3H]gabapentine peut marquer un transporteur d'acides aminés neutres de type système-L dans le cerveau. | Thurlow, RJ., et al. 1993. Eur J Pharmacol. 247: 341-5. PMID: 8307106
- Propriétés conformationnelles des chaînes latérales de L-leucine, L-isoleucine et L-norleucine dans les copolymères de L-lysine. | Arfmann, HA., et al. 1977. Biopolymers. 16: 1815-26. PMID: 890071
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
L-(+)-Norleucine, 100 mg | sc-300860 | 100 mg | $20.00 |
