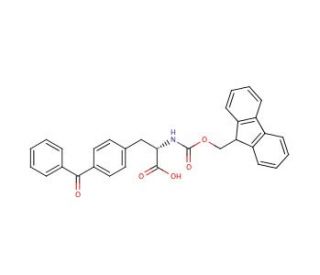
Fmoc-Bpa-OH (CAS 117666-96-3)
ENLACES RÁPIDOS
El Fmoc-Bpa-OH es un compuesto que funciona como un bloque de construcción versátil en la síntesis de péptidos. Actúa como grupo protector del grupo amino de los aminoácidos, permitiendo la desprotección selectiva y las posteriores reacciones de acoplamiento. El mecanismo de acción del Fmoc-Bpa-OH implica la formación de enlaces amida estables con los aminoácidos, lo que permite el ensamblaje paso a paso de péptidos de gran pureza y rendimiento. El Fmoc-Bpa-OH facilita la síntesis de péptidos complejos al proporcionar un medio para controlar la reactividad de grupos funcionales específicos, lo que conduce a la construcción precisa de cadenas peptídicas. Su papel en la síntesis de péptidos implica la protección de los grupos amino, evitando reacciones secundarias no deseadas y garantizando la formación satisfactoria de enlaces peptídicos. El mecanismo de acción de Fmoc-Bpa-OH a nivel molecular permite la síntesis eficiente y controlada de péptidos con secuencias y estructuras a medida, lo que lo convierte en una herramienta útil en la investigación y el desarrollo de la química peptídica.
Fmoc-Bpa-OH (CAS 117666-96-3) Referencias
- Doble papel del proapoptótico BAD en la secreción de insulina y la supervivencia de las células beta. | Danial, NN., et al. 2008. Nat Med. 14: 144-53. PMID: 18223655
- Síntesis y caracterización espectroscópica de ligandos peptídicos de fotoafinidad para estudiar la interacción rodopsina-proteína G. | Chen, Y., et al. 2008. Photochem Photobiol. 84: 831-8. PMID: 18282180
- La histéresis de la compuerta subraya la sensibilización de los canales TRPV3. | Liu, B., et al. 2011. J Gen Physiol. 138: 509-20. PMID: 22006988
- Manipulación de la activación del subtipo de receptor Y de análogos cortos del neuropéptido Y mediante la introducción de carbaboranos. | Hofmann, S., et al. 2013. Neuropeptides. 47: 59-66. PMID: 23352609
- Activación directa de la BAK proapoptótica de longitud completa. | Leshchiner, ES., et al. 2013. Proc Natl Acad Sci U S A. 110: E986-95. PMID: 23404709
- Síntesis química de péptidos unidos a hidrocarburos para la investigación de la interacción proteica y la orientación terapéutica. | Bird, GH., et al. 2011. Curr Protoc Chem Biol. 3: 99-117. PMID: 23801563
- La unión del inhibidor PA1b a las subunidades c y e de la ATPasa vacuolar revela su mecanismo insecticida. | Muench, SP., et al. 2014. J Biol Chem. 289: 16399-408. PMID: 24795045
- La foto-lisina capta las proteínas que se unen a las modificaciones postraduccionales de la lisina. | Yang, T., et al. 2016. Nat Chem Biol. 12: 70-2. PMID: 26689789
- Enfoques Proteómicos Químicos y de Middle-Down para Revelar la Dinámica de la Modificación de la Histona H4 en el Ciclo Celular: Semicuantificación sin etiquetas de las modificaciones peptídicas de la cola de la histona, incluida la fosforilación, y captura altamente sensible de proteínas de unión a PTM de histonas mediante reticulantes fotorreactivos. | Yamamoto, K., et al. 2015. Mass Spectrom (Tokyo). 4: A0039. PMID: 26819910
- Péptidos cortos dirigidos a la integrasa del VIH-1 derivados de una secuencia de la proteína viral R. | Zhao, XZ., et al. 2018. Molecules. 23: PMID: 30049955
- Expresión sin células y fotoentrecruzamiento del receptor humano del neuropéptido Y2. | Kögler, LM., et al. 2019. Front Pharmacol. 10: 176. PMID: 30881304
- Selección de dianas bacterianas y liberación desencadenada por la infección de conjugados antibióticos de colistina. | Tegge, W., et al. 2021. Angew Chem Int Ed Engl. 60: 17989-17997. PMID: 34097810
- La dinámica conformacional vinculada al cierre del dominio y a la unión del sustrato explica el mecanismo de regulación alostérica de ERAP1. | Maben, Z., et al. 2021. Nat Commun. 12: 5302. PMID: 34489420
- Localización del sitio de interacción entre la semaforina-3A y su péptido inhibidor. | Kretschmer, K., et al. 2023. J Pept Sci. 29: e3460. PMID: 36285908
- La vacunación profiláctica y terapéutica protege la salud del esperma de las anomalías inducidas por Chlamydia muridarum. | Bryan, ER., et al. 2023. Biol Reprod. 108: 758-777. PMID: 36799886
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
Fmoc-Bpa-OH, 1 g | sc-223992 | 1 g | $309.00 |
