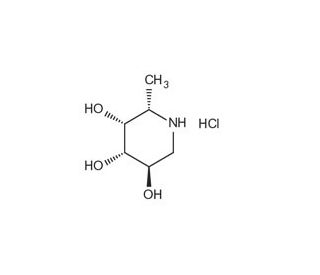
Deoxyfuconojirimycin hydrochloride (CAS 210174-73-5)
Ver las publicaciones del producto (3)
ENLACES RÁPIDOS
Deoxyfuconojirimycin hydrochloride es un análogo del iminosugar fucosa y es un compuesto reconocido por su acción inhibitoria sobre las enzimas glicosidasa. Esta inhibición es particularmente relevante en el estudio del procesamiento y maduración de glicoproteínas dentro del retículo endoplásmico y el aparato de Golgi. Los investigadores aprovechan el deoxyfuconojirimycin hydrochloride para investigar el papel de las glicosidasas en el plegamiento correcto de las glicoproteínas, lo cual tiene implicaciones para entender enfermedades caracterizadas por el mal plegamiento de proteínas. Además, este compuesto se utiliza en la glicobiología para explorar la síntesis y función de glicolípidos y glicoproteínas, así como los efectos patológicos de su síntesis aberrante. La inhibición de las glicosidasas por deoxyfuconojirimycin hydrochloride también es un punto de interés en el estudio de la replicación viral, donde la glicosilación adecuada de las proteínas virales es esencial para el ensamblaje del virus y su infectividad. La acción del compuesto ayuda a dilucidar las complejas vías de interacción entre el huésped y el virus, y la interrupción potencial de estos procesos.
Deoxyfuconojirimycin hydrochloride (CAS 210174-73-5) Referencias
- Fucosiltransferasas en el desarrollo de Schistosoma mansoni. | Marques, ET., et al. 2001. Glycobiology. 11: 249-59. PMID: 11320063
- Conveniente síntesis y evaluación de la actividad inhibidora enzimática de varios derivados N-alquil-, N-fenilalquil- e isourea cíclica de la 5a-carba-alfa-DL-fucopiranosilamina. | Ogawa, S., et al. 2002. Bioorg Med Chem Lett. 12: 2811-4. PMID: 12270152
- Base estructural del mecanismo de reacción catalítica de la nueva 1,2-alfa-L-fucosidasa de Bifidobacterium bifidum. | Nagae, M., et al. 2007. J Biol Chem. 282: 18497-18509. PMID: 17459873
- Las moléculas de alfa-L-fucosa asociadas a la superficie celular modulan la progresión neoplásica del cáncer de mama humano. | Yuan, K., et al. 2008. Pathol Oncol Res. 14: 145-56. PMID: 18553163
- Inhibición de la alfa-L-fucosidasa por derivados de la desoxifuconojirimicina y la desoximannojirimicina. | Winchester, B., et al. 1990. Biochem J. 265: 277-82. PMID: 2137330
- Papel de las alfa-L-fucosidasas asociadas al esperma de ratón en la fecundación. | Phopin, K., et al. 2013. Mol Reprod Dev. 80: 273-85. PMID: 23426913
- Digestión de carbohidratos en garrapatas y una α-L-fucosidasa digestiva. | Moreti, R., et al. 2013. J Insect Physiol. 59: 1069-75. PMID: 23994295
- Caracterización de una α-l-fucosidasa del patógeno periodontal Tannerella forsythia. | Megson, ZA., et al. 2015. Virulence. 6: 282-92. PMID: 25831954
- Un dominio de lectina de tipo F dirige la actividad de la alfa-l-fucosidasa de Streptosporangium roseum. | Bishnoi, R., et al. 2018. Glycobiology. 28: 860-875. PMID: 30169639
- Desarrollo de un método UHPLC-MS para la detección de inhibidores de la α-L-1,3-fucosidasa. | Liu, T., et al. 2019. Anal Bioanal Chem. 411: 1467-1477. PMID: 30706074
- Las estructuras crio-EM de la fucosidasa humana FucA1 revelan el reconocimiento de sustratos y la catálisis. | Armstrong, Z., et al. 2022. Structure. 30: 1443-1451.e5. PMID: 35907402
- Purificación y caracterización de alfa-L-fucosidasa a partir de sobrenadante de cultivo de células de ovario de hámster chino. | Gramer, MJ., et al. 1994. Glycobiology. 4: 611-6. PMID: 7881175
- La unión del esperma bovino al epitelio oviductal implica el reconocimiento de la fucosa. | Lefebvre, R., et al. 1997. Biol Reprod. 56: 1198-204. PMID: 9160719
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
Deoxyfuconojirimycin hydrochloride, 1 mg | sc-205644 | 1 mg | $112.00 | |||
Deoxyfuconojirimycin hydrochloride, 5 mg | sc-205644A | 5 mg | $265.00 | |||
Deoxyfuconojirimycin hydrochloride, 25 mg | sc-205644B | 25 mg | $479.00 | |||
Deoxyfuconojirimycin hydrochloride, 50 mg | sc-205644C | 50 mg | $694.00 | |||
Deoxyfuconojirimycin hydrochloride, 100 mg | sc-205644D | 100 mg | $1019.00 |
