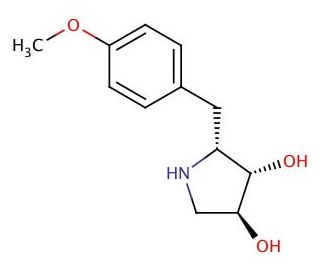
Deacetylanisomycin (CAS 27958-06-1)
ENLACES RÁPIDOS
La deacetilanisomicina, identificada con el número CAS 27958-06-1, es un derivado de la anisomicina, un conocido antibiótico que funciona como inhibidor de la síntesis de proteínas. Este compuesto difiere de la anisomicina por la eliminación de un grupo acetilo, una modificación que repercute en su actividad biológica y en su interacción con las dianas celulares. La deacetilanisomicina actúa uniéndose a la subunidad ribosómica 60S, influyendo específicamente en el centro de la peptidil transferasa dentro de la subunidad ribosómica grande. Esta unión altera la función normal del ribosoma, lo que conduce a la inhibición de la formación de enlaces peptídicos, que es un paso crucial en el proceso de traducción de la síntesis de proteínas. En consecuencia, esta interferencia detiene eficazmente la fase de elongación de la síntesis de proteínas, inhibiendo así la producción total de proteínas en las células. En contextos de investigación, la deacetilanisomicina se utiliza principalmente para estudiar los mecanismos de la síntesis de proteínas a nivel molecular y para explorar las respuestas celulares a la traducción inhibida, como las vías de respuesta al estrés, incluida la vía de señalización MAPK. Los investigadores también emplean la deacetilanisomicina para investigar los aspectos estructurales y funcionales de los componentes ribosomales, proporcionando información sobre cómo las modificaciones en los antibióticos dirigidos a los ribosomas afectan a su interacción con los ribosomas y a sus posteriores actividades biológicas. Esta investigación es crucial para comprender los procesos fundamentales que controlan el crecimiento celular y la respuesta al estrés ambiental.
Deacetylanisomycin (CAS 27958-06-1) Referencias
- La memoria dependiente de la síntesis de proteínas y la mejora neuronal en Hermissenda dependen de parámetros de entrenamiento y retención. | Ramirez, RR., et al. 1998. Learn Mem. 4: 462-77. PMID: 10701872
- Síntesis estereodivergentes de derivados de anisomicina a partir de D-tirosina. | Kim, JH., et al. 2005. J Org Chem. 70: 4082-7. PMID: 15876100
- Comparación de las actividades in vitro de los cuasinoides con la actividad contra Plasmodium falciparum, la anisomicina y algunos otros inhibidores de la síntesis de proteínas eucariotas. | Ekong, RM., et al. 1990. Biochem Pharmacol. 40: 297-301. PMID: 2198027
- La inhibición de la síntesis proteica bloquea el aumento a largo plazo de los potenciales generadores producidos por el condicionamiento in vivo de un solo ensayo en Hermissenda. | Crow, T. and Forrester, J. 1990. Proc Natl Acad Sci U S A. 87: 4490-4. PMID: 2352932
- La inhibición de la síntesis proteica prolonga la reducción de las corrientes de K+ mediada por Ca2+ en neuronas de moluscos. | Alkon, DL., et al. 1987. Proc Natl Acad Sci U S A. 84: 6948-52. PMID: 3477819
- Unión de (3H)anisomicina a ribosomas eucariotas. | Barbacid, M. and Vazquez, D. 1974. J Mol Biol. 84: 603-23. PMID: 4601392
- Necesidad de síntesis proteica en la regulación del ritmo circadiano por la serotonina. | Eskin, A., et al. 1984. Proc Natl Acad Sci U S A. 81: 7637-41. PMID: 6095312
- Necesidad de síntesis proteica del reloj circadiano de la Aplysia. Probado con derivados activos e inactivos del inhibidor anisomicina. | Jacklet, JW. 1980. J Exp Biol. 85: 33-42. PMID: 7373209
- La anisomicina desensibiliza selectivamente los componentes de señalización implicados en la activación de la cinasa de estrés y la inducción de fos y jun. | Hazzalin, CA., et al. 1998. Mol Cell Biol. 18: 1844-54. PMID: 9528756
- Desarrollo y validación de métodos LC-UV y LC-MS/MS indicadores de estabilidad para el análisis cuantitativo de anisomicina y la identificación de productos de degradación. | Tolić, et al. 2018. Brazilian Journal of Pharmaceutical Sciences. 54: e17491.
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
Deacetylanisomycin, 5 mg | sc-391507 | 5 mg | $327.00 |
