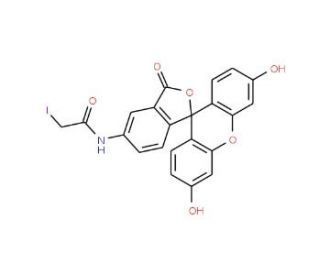
5-(Iodoacetamido)fluorescein (CAS 63368-54-7)
ENLACES RÁPIDOS
La 5-(yodoacetamido)fluoresceína es una molécula utilizada en la investigación bioquímica para marcar proteínas, péptidos y otras biomoléculas. Su capacidad para unirse covalentemente a los grupos tiol de los residuos de cisteína a través de su grupo funcional yodoacetamida explica su frecuente aplicación en microscopía de fluorescencia y citometría de flujo. Este compuesto es especialmente valioso para investigar la estructura y la dinámica de las proteínas, ya que la fracción de fluoresceína unida proporciona una señal fluorescente que puede detectarse y cuantificarse. En estudios de interacción proteína-proteína, la 5-(Yodoacetamido)fluoresceína facilita la visualización de formaciones complejas, ayudando así a dilucidar mecanismos moleculares. También se utiliza en el estudio de actividades enzimáticas y cambios conformacionales en proteínas, ya que las propiedades fluorescentes del compuesto cambian al unirse, proporcionando una medida de los procesos bioquímicos en tiempo real.
5-(Iodoacetamido)fluorescein (CAS 63368-54-7) Referencias
- Modulación del estado redox de la tubulina por el sistema glutatión/glutaredoxina reductasa. | Landino, LM., et al. 2004. Biochem Biophys Res Commun. 314: 555-60. PMID: 14733943
- Modulación redox de tau y de la proteína-2 asociada a microtúbulos por el sistema glutatión/glutaredoxina reductasa. | Landino, LM., et al. 2004. Biochem Biophys Res Commun. 323: 112-7. PMID: 15351709
- Deslizamiento y fuga de protones inducidos por la luz en la membrana del tilacoide. | Richter, M., et al. 2004. J Plant Physiol. 161: 1325-37. PMID: 15658803
- Determinación sensible y selectiva de glutatión en bacterias probióticas mediante electroforesis capilar-fluorescencia inducida por láser. | Musenga, A., et al. 2007. Anal Bioanal Chem. 387: 917-24. PMID: 17203251
- Modificación de tioles de proteínas por el anión peroxinitrito y donantes de óxido nítrico. | Landino, LM. 2008. Methods Enzymol. 440: 95-109. PMID: 18423212
- La fluoresceína como etiqueta versátil para mejorar la selectividad en el análisis de proteínas/péptidos que contienen cisteína mediante espectrometría de masas. | Chen, SH., et al. 2008. Anal Chem. 80: 5251-9. PMID: 18512949
- Inhibición de la polimerización de la tubulina por el ácido hipocloroso y las cloraminas. | Landino, LM., et al. 2011. Free Radic Biol Med. 50: 1000-8. PMID: 21256958
- Mecanismo cinético de los cambios controlados por Ca²⁺ de la troponina I esquelética en las miofibrillas del psoas. | Lopez-Davila, AJ., et al. 2012. Biophys J. 103: 1254-64. PMID: 22995498
- La oxidación de las cisteínas de la tubulina por el ácido hipotiociánico inhibe la polimerización de los microtúbulos. | Clark, HM., et al. 2014. Arch Biochem Biophys. 541: 67-73. PMID: 24215946
- Cambios proteómicos redox en el hongo patógeno Trichosporon asahii por exposición al arsénico: identificación de respuestas proteínicas al estrés oxidativo inducido por metales en un aislado muestreado ambientalmente. | Ilyas, S., et al. 2014. PLoS One. 9: e102340. PMID: 25062082
- Evidencia de reacciones de intercambio tiol/disulfuro entre la tubulina y la gliceraldehído-3-fosfato deshidrogenasa. | Landino, LM., et al. 2014. Cytoskeleton (Hoboken). 71: 707-18. PMID: 25545749
- Interacciones proteína-proteína en la activación por contacto de la coagulación sanguínea. Unión del kininógeno de alto peso molecular y de la cadena ligera de kininógeno marcada con 5-(iodoacetamido) fluoresceína a la precalicreína, la calicreína y las cadenas pesadas y ligeras separadas de la calicreína. | Bock, PE., et al. 1985. J Biol Chem. 260: 12434-43. PMID: 3850090
- Conformación de los colorantes de xanteno en el sitio de unión del sulfhidrilo 1 de la miosina. 2. | Ajtai, K. and Burghardt, TP. 1995. Biochemistry. 34: 15943-52. PMID: 8519751
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
5-(Iodoacetamido)fluorescein, 25 mg | sc-214304 | 25 mg | $162.00 | |||
5-(Iodoacetamido)fluorescein, 100 mg | sc-214304A | 100 mg | $537.00 | |||
5-(Iodoacetamido)fluorescein, 250 mg | sc-214304B | 250 mg | $1200.00 |
