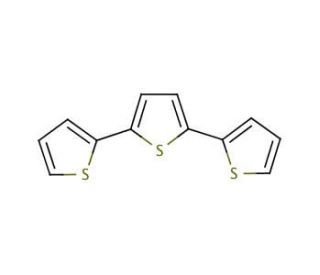
2,2′:5′,2′′-Terthiophene (CAS 1081-34-1)
ENLACES RÁPIDOS
2,2':5',2''-Terthiophene (2,2':5',2''-TTP) es un miembro de la familia de compuestos orgánicos de tiofeno. Su estructura única presenta un anillo de cinco miembros que conecta dos átomos de azufre y un anillo de dos miembros que conecta dos átomos de oxígeno. Ampliamente estudiado por sus características notables, 2,2':5',2''-TTP exhibe una alta solubilidad en disolventes orgánicos, lo que lo hace de gran interés para posibles aplicaciones en electrónica orgánica y optoelectrónica.En el ámbito de la electrónica orgánica y la optoelectrónica, 2,2':5',2''-TTP toma el centro del escenario. Sirve como un material activo crucial en dispositivos como transistores orgánicos de efecto campo (OFETs), diodos orgánicos emisores de luz (OLEDs) y células fotovoltaicas orgánicas (OPVs). Juega un papel fundamental en el desarrollo de sensores, en particular sensores electroquímicos, capaces de detectar diversas sustancias como glucosa, amoníaco y óxido nítrico. Uno de sus atributos clave radica en su capacidad para actuar como donante de electrones, facilitando interacciones fuertes con otras moléculas, especialmente aquellas encontradas en los ámbitos de la electrónica orgánica y la optoelectrónica.
2,2′:5′,2′′-Terthiophene (CAS 1081-34-1) Referencias
- Transformaciones fotoinducidas en láminas delgadas de 2,2':5',2''-tertiofeno sobre plata. | Alaverdyan, Y., et al. 2006. Phys Chem Chem Phys. 8: 1445-50. PMID: 16633627
- síntesis electiva y eficaz de derivados fototóxicos de 2, 2′: 5′, 2 ″ derivados de tertiofeno con un sustituyente funcional en la posición 3′ o 5 | Rossi, R., Carpita, A., Ciofalo, M., & Lippolis, V. 1991. Tetrahedron. 47(39): 8443-8460.
- Cruce intersistema singlete-triplete en 2, 2′: 5′, 2 ″-tertiofeno y algunos de sus derivados. | Rossi, R., Ciofalo, M., Carpita, A., & Ponterini, G. 1993. Journal of Photochemistry and Photobiology A: Chemistry. 70(1): 59-67.
- Estudio mecanístico de la fotooxidación del escualeno sensibilizado con 2, 2′: 5′, 2 ″-Tertiofeno y 2, 2′-Bitiofeno | Fujita, H., Tokiwa, K., Sayama, K., Mori, H., & Sasaki, M. 1993. Bulletin of the Chemical Society of Japan. 66(10): 2960-2964.
- Reacciones de adición oxidativa de 2, 2′-bitiofeno y 2, 2′: 5′, 2 ″-tertiofeno con grupos trinucleares de hierro, rutenio y osmio | Arce, A. J., Arrojo, P., De Sanctis, Y., Márquez, M., & Deeming, A. J. 1994. Journal of organometallic chemistry. 479(1-2): 159-164.
- Estudio teórico del 2, 2′; 5′, 2 ″-tertiofeno (α-T) y sus análogos. Part 1. Correlación de la estructura electrónica y las energías con la fototoxicidad herbicida. | Friedman, D. C., & Friedman, P. 1995. Journal of Molecular Structure: THEOCHEM,. 333(1-2): 71-78.
- Investigaciones teóricas sobre defectos bipolarónicos positivos en oligotiofenos: Estructuras y espectros vibracionales de 2,2′-bitiofeno y 2,2′:5′,2″-tertiofeno doblemente cargados | Ehrendorfer, C., & Karpfen, A. 1995. Vibrational Spectroscopy. 8(2): 293-303.
- Espectros estacionarios y resueltos en el tiempo de 2, 2′: 5′, 2 ″-tertiofeno | Yang, A., Hughes, S., Kuroda, M., Shiraishi, Y., & Kobayashi, T. 1997. Chemical physics letters. 280(5-6): 475-480.
- Nuevos derivados difenilfosfínicos del 2,2′-bitiofeno, 2,2′:5′,2″-tertiofeno, 2-(2′-tienil)piridina y 2,6-di-2′-tienilpiridina. Estructuras cristalinas de 5,5′-bis(difenilfosfino)-2,2′-bitiofeno, difenil{5-[6′-(difenilfosfino)-2′-piridil]-2-tienil}fosfina y 2,6-bis[5′-(difenilfosfino)-2′-tienil]piridina. | Field, J. S., Haines, R. J., Lakoba, E. I., & Sosabowski, M. H. 2001. Journal of the Chemical Society, Perkin Transactions 1. (24): 3352-3360.
- Electropolimerización de 2,2′:5′,2″ tertiofeno en una interfaz líquido-líquido electrificada | Gorgy, K., Fusalba, F., Evans, U., Kontturi, K., & Cunnane, V. J. 2001. Synthetic metals. 125(3): 365-373.
- Estudio espectroelectroquímico de la polimerización de 2,2':5',2''-tertiofeno en una interfase líquido/líquido controlada por iones determinantes del potencial | Evans-Kennedy, U., Clohessy, J., & Cunnane, V. J. 2004. Macromolecules. 37(10): 3630-3634.
- Copolimerización electroquímica de carbazol y 2, 2′: 5′-2 ″tertiofeno: caracterización y aplicación en microcondensadores. | Ates, M., & Eren, N. 2014. Iranian Polymer Journal. 23: 581-589.
- Deposición de vapor asistida por líquido iónico y control de polimorfos de cristales de 2, 2′: 5′, 2 ″-tertiofeno cristales | Okawara, K., Maruyama, S., & Matsumoto, Y. 2019. Japanese Journal of Applied Physics. 58(8): 085503.
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
2,2′:5′,2′′-Terthiophene, 1 g | sc-256272 | 1 g | $112.00 |
