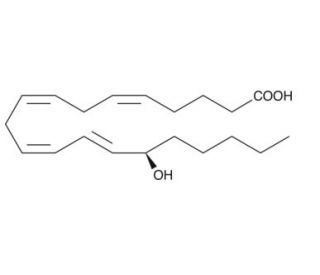
15(R)-HETE (CAS 83603-31-0)
ENLACES RÁPIDOS
El 15(R)-HETE, con el número CAS 83603-31-0, es un enantiómero del ácido 15-hidroxieicosatetraenoico, que se distingue específicamente por la configuración R del grupo hidroxilo en el decimoquinto carbono de la cadena eicosanoide. Este compuesto se sintetiza mediante la acción de la 15-lipoxigenasa sobre el ácido araquidónico. En el ámbito de la investigación bioquímica, el 15(R)-HETE es especialmente apreciado por su papel en la elucidación de los mecanismos subyacentes a la regulación de procesos celulares como la inflamación, la señalización celular y la modulación de los canales iónicos. Las acciones específicas del 15(R)-HETE incluyen influir en el comportamiento de varias vías de señalización que son críticas para la supervivencia celular, la diferenciación y la respuesta al estrés oxidativo. Los investigadores utilizan este compuesto para estudiar sus efectos sobre los niveles de calcio intracelular y su interacción con receptores específicos y proteínas implicadas en la transducción de señales. Este enfoque ayuda a desentrañar las complejas interacciones entre los mediadores lipídicos y los mecanismos celulares, mejorando la comprensión de cómo la señalización lipídica contribuye a la regulación de los procesos fisiológicos. Al investigar los papeles funcionales del 15(R)-HETE, los científicos adquieren conocimientos sobre las interacciones moleculares detalladas que rigen las respuestas y adaptaciones celulares, contribuyendo significativamente al campo más amplio de la biología celular y molecular.
15(R)-HETE (CAS 83603-31-0) Referencias
- 15-Lipoxigenasa en la inflamación glomerular. | Montero, A. and Badr, KF. 2000. Exp Nephrol. 8: 14-9. PMID: 10644878
- Requisitos espaciales para la síntesis del ácido 15-(R)-hidroxi-5Z,8Z,11Z, 13E-eicosatetraenoico dentro del sitio activo de la ciclooxigenasa de la COX-2 murina. Por qué la COX-1 acetilada no sintetiza 15-(R)-hete. | Rowlinson, SW., et al. 2000. J Biol Chem. 275: 6586-91. PMID: 10692466
- Mediadores antiinflamatorios endógenos del araquidonato en neutrófilos humanos. | Vachier, I., et al. 2002. Biochem Biophys Res Commun. 290: 219-24. PMID: 11779156
- Daño del ADN mediado por la ciclooxigenasa-2. | Lee, SH., et al. 2005. J Biol Chem. 280: 28337-46. PMID: 15964853
- La 15-epi-lipoxina A4 desencadenada por la aspirina predice la ciclooxigenasa-2 en los pulmones de ratones tratados con LPS pero no en la circulación: implicaciones para un ensayo clínico. | Kirkby, NS., et al. 2013. FASEB J. 27: 3938-46. PMID: 23792301
- Aspirina y mediadores lipídicos en el sistema cardiovascular. | Schrör, K. and Rauch, BH. 2015. Prostaglandins Other Lipid Mediat. 121: 17-23. PMID: 26201059
- Análisis de HETEs en sangre total humana mediante UHPLC-ECAPCI/HRMS quiral. | Mazaleuskaya, LL., et al. 2018. J Lipid Res. 59: 564-575. PMID: 29301865
- La actividad ciclooxigenasa residual de la COX-2 acetilada con aspirina forma 15 R-prostaglandinas que inhiben la agregación plaquetaria. | Giménez-Bastida, JA., et al. 2019. FASEB J. 33: 1033-1041. PMID: 30096040
- Caracterización de sitios subcelulares específicos de unión del ácido 15-hidroxieicosatetraenoico (15-HETE) en células leucémicas basófilas de rata. | Kang, LT. and Vanderhoek, JY. 1995. Biochim Biophys Acta. 1256: 297-304. PMID: 7786891
- La mutación de la serina-516 en la prostaglandina G/H sintasa-2 humana a metionina o la acetilación con aspirina de este residuo estimula la síntesis de 15-R-HETE. | Mancini, JA., et al. 1994. FEBS Lett. 342: 33-7. PMID: 8143845
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
15(R)-HETE, 25 µg | sc-205032 | 25 µg | $139.00 | |||
15(R)-HETE, 50 µg | sc-205032A | 50 µg | $199.00 |
