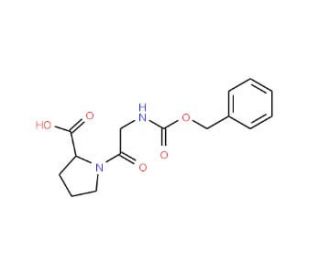
Z-Gly-Pro-OH (CAS 1160-54-9)
Direktverknüpfungen
Z-Gly-Pro-OH ist ein zyklischer Dipeptid, bestehend aus zwei Aminosäuren, die durch eine Peptidbindung miteinander verbunden sind. Es spielt eine entscheidende Rolle in zahlreichen Prozessen und erregt in der wissenschaftlichen Forschung großes Interesse. Die wissenschaftlichen Forschungsanwendungen von Z-Gly-Pro-OH waren vielfältig und wirkungsvoll. Forscher haben es umfangreich genutzt, um die Strukturen und Funktionen von Proteinen, Peptiden und Enzymen zu erforschen. Darüber hinaus war es ein wertvolles Asset bei der Untersuchung von Zellmembranen und Signalwegen und hat wichtige Einblicke in zelluläre Prozesse geliefert. Darüber hinaus kann der Beitrag von Z-Gly-Pro-OH zum Verständnis von DNA, RNA und metabolischen Wegen nicht übersehen werden. In Bezug auf seine Wirkungsmechanismen bestehen noch einige Unsicherheiten. Es wird jedoch postuliert, dass das zyklische Dipeptid an bestimmte Proteine und Peptide bindet und dadurch eine Kaskade von Interaktionen auslöst, die wichtige zelluläre Prozesse regulieren. So wurde beobachtet, dass es sich an bestimmte Enzyme bindet und so die Katalyse der Bildung neuer Moleküle oder den Abbau bestehender Moleküle erleichtert.
Z-Gly-Pro-OH (CAS 1160-54-9) Literaturhinweise
- Die nicht-katalytische Beta-Propeller-Domäne der Prolyl-Oligopeptidase verstärkt die katalytische Fähigkeit der Peptidase-Domäne. | Szeltner, Z., et al. 2000. J Biol Chem. 275: 15000-5. PMID: 10747969
- Substratabhängige Kompetenz der katalytischen Triade der Prolyl-Oligopeptidase. | Szeltner, Z., et al. 2002. J Biol Chem. 277: 44597-605. PMID: 12228249
- Charakterisierung des aktiven Zentrums einer neu entdeckten und potenziell bedeutenden Post-Prolin-spaltenden Endopeptidase namens ZIP mittels LC-UV-MS. | McMahon, G., et al. 2003. Analyst. 128: 670-5. PMID: 12866886
- Analoga des neuroprotektiven Tripeptids Gly-Pro-Glu (GPE): Synthese und Struktur-Wirkungsbeziehungen. | Alonso De Diego, SA., et al. 2005. Bioorg Med Chem Lett. 15: 2279-83. PMID: 15837309
- Eigenschaften des Prolyl-Oligopeptidase-Homologs aus Pyrococcus furiosus. | Juhász, T., et al. 2006. FEBS Lett. 580: 3493-7. PMID: 16714022
- Liganden-induzierte Konformationsänderungen in Prolyl-Oligopeptidase: ein kinetischer Ansatz. | Van Elzen, R., et al. 2017. Protein Eng Des Sel. 30: 217-224. PMID: 28062644
- Decarboxylierung von Carbonsäuren bei Raumtemperatur mit Hilfe von Photoredox-Katalysatoren und Cyanobenziodoxolonen: ein abweichender Mechanismus im Vergleich zur Alkynylierung. | Le Vaillant, F., et al. 2017. Chem Sci. 8: 1790-1800. PMID: 28451301
- Clostridium histolyticum Kollagenase: Entwicklung neuer Thioester-, Fluorogen- und Depsipeptid-Substrate und neuer Inhibitoren. | Vencill, CF., et al. 1985. Biochemistry. 24: 3149-57. PMID: 2992578
- Photochemische Strain-Release-getriebene Cyclobutylierung von C(sp3)-zentrierten Radikalen. | Ernouf, G., et al. 2020. Angew Chem Int Ed Engl. 59: 2618-2622. PMID: 31599038
- Studien zu Substratanforderungen, kinetischen Eigenschaften und konkurrierenden Inhibitoren der Enzyme, die TRH im Rattenhirn abbauen. | Busby, WH., et al. 1982. Brain Res. 242: 261-70. PMID: 6126250
- NMR-Untersuchungen eines freien und geschützten Tetrapeptids Glycyl-L-Prolylglycylglycin in Beta-Turn-unterstützender Umgebung. | Perly, B., et al. 1983. Biopolymers. 22: 1853-68. PMID: 6616010
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Z-Gly-Pro-OH, 1 g | sc-296758 | 1 g | $70.00 | |||
Z-Gly-Pro-OH, 5 g | sc-296758A | 5 g | $206.00 |
