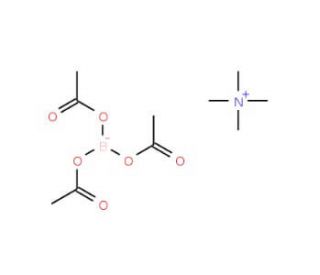
Tetramethylammonium triacetoxyborohydride (CAS 109704-53-2)
Direktverknüpfungen
Tetramethylammoniumtriacetoxyborohydrid (TMAB) ist eine leistungsstarke organische Verbindung, die in der synthetischen organischen Chemie weit verbreitet ist. Es dient als robustes Reduktionsmittel, das hauptsächlich zur Umwandlung von Aldehyden und Ketonen in ihre jeweiligen Alkohole verwendet wird. Darüber hinaus spielt TMAB eine entscheidende Rolle bei der Konstruktion verschiedener organischer Moleküle wie Aminen, Ester und Amide. In der synthetischen organischen Chemie ist die weitverbreitete Anwendung von Tetramethylammoniumtriacetoxyborohydrid offensichtlich. Seine Verwendung umfasst die Erstellung einer Vielzahl organischer Entitäten, von Aminen, Ester und Amiden bis hin zu Polymeren und Farbstoffen. Die Kapazität von Tetramethylammoniumtriacetoxyborohydrid als leistungsstarkes Reduktionsmittel ist unverkennbar, insbesondere in seiner Fähigkeit, Aldehyde und Ketonen in ihre entsprechenden Alkohole umzuwandeln. Die zugrunde liegende Mechanik dieser Transformation beinhaltet die orchestrierte Übertragung von Elektronen vom Boratom auf das Carbonyl-Moiety des Aldehyds oder Keton, was schließlich zur Reduktion der Carbonylgruppe zu einem Alkohol führt.
Tetramethylammonium triacetoxyborohydride (CAS 109704-53-2) Literaturhinweise
- Synthetische Studien zu (-)-FR901483 unter Verwendung einer konjugierten Allylierung zum Einbau des quaternären C-1-Kohlenstoffs. | Gotchev, DB. and Comins, DL. 2006. J Org Chem. 71: 9393-402. PMID: 17137366
- Atomökonomische und stereoselektive Synthesen der Ring-A- und B-Untereinheiten der Bryostatine. | Trost, BM., et al. 2011. Chemistry. 17: 9777-88. PMID: 21774000
- Entwicklung von enantioselektiven Synthesewegen zu (-)-Kinamycin F und (-)-Lomaiviticin-Aglykon. | Woo, CM., et al. 2012. J Am Chem Soc. 134: 17262-73. PMID: 23030272
- Stereokontrolle bei Palladium-katalysierten propargylischen Substitutionen: Kinetische Auflösung zur Erzeugung von enantioangereicherten 1,5-Eninen und Propargylacetaten. | Ardolino, MJ., et al. 2013. Adv Synth Catal. 355: 3413-3419. PMID: 24839434
- Diacyltransferase-Aktivität und Kettenlängenspezifität von Mycobacterium tuberculosis PapA5 bei der Synthese von Alkyl-β-Diol-Lipiden. | Touchette, MH., et al. 2015. Biochemistry. 54: 5457-68. PMID: 26271001
- Synthese eines vereinfachten Triazol-Analogons von Pateamin A. | Hemi Cumming, A., et al. 2016. Org Biomol Chem. 14: 5117-27. PMID: 27180995
- Identifizierung neuartiger Acetylcholinesterase-Inhibitoren durch virtuelles Screening auf Pharmakophorbasis, molekulares Docking und Bioassay. | Jang, C., et al. 2018. Sci Rep. 8: 14921. PMID: 30297729
- Überlegene zelluläre Aktivitäten von Azido- gegenüber Amino-funktionalisierten Liganden für konstruierte preQ1-Riboswitches in E.coli. | Neuner, E., et al. 2018. RNA Biol. 15: 1376-1383. PMID: 30332908
- Totalsynthesen der Xiamycine A, C, F, H und Oridamycin A und vorläufige Bewertung ihrer Anti-Pilz-Eigenschaften. | Pfaffenbach, M., et al. 2019. Angew Chem Int Ed Engl. 58: 15304-15308. PMID: 31419367
- Leichte Synthese von Saikosaponinen. | Wang, Z., et al. 2021. Molecules. 26: PMID: 33808330
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Tetramethylammonium triacetoxyborohydride, 10 g | sc-258237 | 10 g | $203.00 |
