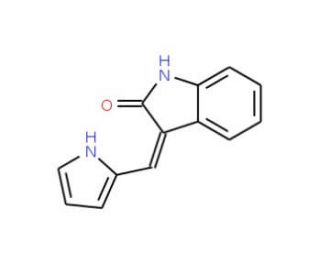
Molecular structure of Oxindole I
Oxindole I
See product citations (2)
Alternate Names:
3-(1H-Pyrrol-2-ylmethylene)-1,3-dihydroindol-2-one
Application:
Oxindole I is a potent, selective inhibitor of VEGF
Molecular Weight:
210.2
Molecular Formula:
C13H10N2O
For Research Use Only. Not Intended for Diagnostic or Therapeutic Use.
* Refer to Certificate of Analysis for lot specific data.
QUICK LINKS
Ordering Information
Product Citations
Description
Technical Information
Safety Information
SDS & Certificate of Analysis
Oxindole I is a potent and selective inhibitor of vascular endothelial growth factor (VEGF) receptor tyrosine kinase Flk-1 (fetal liver kinase-1 IC50 = 390 nM). Also, to a lesser extent, it inhibits PDGFR (platelet derived growth factor receptor) kinase (IC50 = 12 muM). However, Oxindole I does not affect EGFR, HER2, and IGF-1R even at high concentrations (>100 muM). Oxindole I also inhibits cyclin D1/Cdk4 enzyme (IC50 = 4.9 muM) preferentially over cyclin E/Cdk2 (IC50 = 10 muM) and cyclin B/Cdk1 (IC50 = 10.2 muM).
Oxindole I References
- Characterization of novel inhibitors of cyclin-dependent kinases. | Kent, LL., et al. 1999. Biochem Biophys Res Commun. 260: 768-74. PMID: 10403840
- DoMCoSAR: a novel approach for establishing the docking mode that is consistent with the structure-activity relationship. Application to HIV-1 protease inhibitors and VEGF receptor tyrosine kinase inhibitors. | Vieth, M. and Cummins, DJ. 2000. J Med Chem. 43: 3020-32. PMID: 10956210
- Novel 5-aryl-1,3-dihydro-indole-2-thiones. potent, orally active progesterone receptor agonists. | Fensome, A., et al. 2003. Bioorg Med Chem Lett. 13: 1317-20. PMID: 12657272
- Generation of FGF reporter transgenic zebrafish and their utility in chemical screens. | Molina, GA., et al. 2007. BMC Dev Biol. 7: 62. PMID: 17553162
- AR inhibitors identified by high-throughput microscopy detection of conformational change and subcellular localization. | Jones, JO., et al. 2009. ACS Chem Biol. 4: 199-208. PMID: 19236099
- Phenyliodine bis(trifluoroacetate)-mediated oxidative C-C bond formation: synthesis of 3-hydroxy-2-oxindoles and spirooxindoles from anilides. | Wang, J., et al. 2012. Org Lett. 14: 2210-3. PMID: 22497343
- Highly Enantioselective Tandem Michael Addition of Tryptamine-Derived Oxindoles to Alkynones: Concise Synthesis of Strychnos Alkaloids. | He, W., et al. 2018. Angew Chem Int Ed Engl. 57: 3806-3809. PMID: 29418057
- Dual inhibition of Kif15 by oxindole and quinazolinedione chemical probes. | Dumas, ME., et al. 2019. Bioorg Med Chem Lett. 29: 148-154. PMID: 30528696
Inhibitor of:
Cdk1, Cdk2, Cdk4, cyclin B, cyclin D1, cyclin E, Flk-1, PDGFR, and Protease.Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
Oxindole I, 10 mg | sc-222104 | 10 mg | $273.00 |
