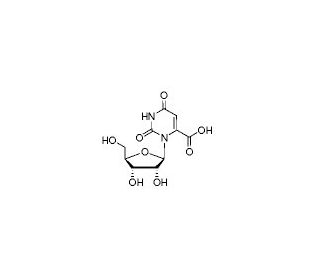
Orotidine (CAS 314-50-1)
Direktverknüpfungen
Orotidin wird in der biochemischen Forschung ausgiebig genutzt, insbesondere wegen seiner Beteiligung an der Pyrimidin-Biosynthese. Diese Verbindung wird in Studien verwendet, die sich mit den enzymatischen Wegen der Nukleotidsynthese befassen, wo sie als Substrat im Umwandlungsprozess fungiert, der durch die Orotat-Phosphoribosyltransferase und die Orotidin-5'-phosphat-Decarboxylase vermittelt wird. Die Forschung mit Orotidin zielt häufig darauf ab, die Mechanismen dieser Enzyme aufzuklären und Einblicke in die genetische Regulierung und Stoffwechselkontrolle zu gewinnen. Darüber hinaus wird Orotidin bei der Untersuchung von Stoffwechselstörungen im Zusammenhang mit der Nukleotidbiosynthese eingesetzt, was ein tieferes Verständnis von Krankheitszuständen auf molekularer Ebene ermöglicht. Darüber hinaus wird die Rolle von Orotidin bei der Synthese und Regulierung von RNA und DNA untersucht, wodurch das Wissen über zelluläre Replikations- und Transkriptionsprozesse erweitert wird.
Orotidine (CAS 314-50-1) Literaturhinweise
- Die strukturelle Grundlage für die bemerkenswerte katalytische Leistungsfähigkeit der Orotidin-5'-monophosphat-Decarboxylase. | Begley, TP., et al. 2000. Curr Opin Struct Biol. 10: 711-8. PMID: 11114509
- Katalyse durch Konformationsänderung des Enzyms am Beispiel der Orotidin-5'-monophosphat-Decarboxylase. | Gao, J. 2003. Curr Opin Struct Biol. 13: 184-92. PMID: 12727511
- Hemmung der Orotidin-5'-Monophosphat-Decarboxylase - Entdeckungen und Lehren. | Kotra, LP. and Pai, EF. 2008. Nucleic Acids Symp Ser (Oxf). 85-6. PMID: 18776265
- Semi-gezielte Analyse von Metaboliten mittels Kapillarfluss-Ionenchromatographie gekoppelt mit hochauflösender Massenspektrometrie. | Burgess, K., et al. 2011. Rapid Commun Mass Spectrom. 25: 3447-52. PMID: 22002700
- Orotidin-5'-monophosphat-Decarboxylase: Stabilisierung des Übergangszustands durch entfernte Protein-Phosphodianion-Wechselwirkungen. | Amyes, TL., et al. 2012. Biochemistry. 51: 4630-2. PMID: 22620855
- Neue Cytidin-basierte Orotidin-5'-Monophosphat-Decarboxylase-Inhibitoren mit einer ungewöhnlichen Wendung. | Purohit, MK., et al. 2012. J Med Chem. 55: 9988-97. PMID: 22991951
- Katalyse durch Orotidin-5'-monophosphat-Decarboxylase: Wirkung von 5-Fluor- und 4'-Substituenten auf die Decarboxylierung von zweiteiligen Substraten. | Goryanova, B., et al. 2013. Biochemistry. 52: 537-46. PMID: 23276261
- Phylogenetische Analyse zeigt eine kryptische Art Blastomyces gilchristii, sp. nov. innerhalb des humanpathogenen Pilzes Blastomyces dermatitidis. | Brown, EM., et al. 2013. PLoS One. 8: e59237. PMID: 23533607
- Orotidinmonophosphat-Decarboxylase - ein faszinierendes Arbeitstier-Enzym mit therapeutischem Potenzial. | Fujihashi, M., et al. 2015. J Genet Genomics. 42: 221-34. PMID: 26059770
- Bifunktionelle Aktivität von fusionierter Plasmodium falciparum Orotat-Phosphoribosyltransferase und Orotidin-5'-Monophosphat-Decarboxylase. | Paojinda, P., et al. 2018. Parasitol Int. 67: 79-84. PMID: 28389349
- Orotidin-haltige RNA: Implikationen für die hierarchische Selektion (Systemchemie Emergenz) von RNA. | Kim, EK., et al. 2017. Chemistry. 23: 12668-12675. PMID: 28708927
- Enzymarchitektur: Aufbau der aktiven Orotidin-5'-Monophosphat-Decarboxylase durch substratinduzierte Konformationsänderungen. | Reyes, AC., et al. 2017. J Am Chem Soc. 139: 16048-16051. PMID: 29058891
- Eine tiefgreifende computergestützte Studie zur Priorisierung von Naturstoff-Inhibitoren gegen das P. falciparum Orotidin-5-Monophosphat-Decarboxylase-Enzym. | Manhas, A., et al. 2020. J Biomol Struct Dyn. 38: 2704-2716. PMID: 31304874
- Die Unterbrechung oder reduzierte Expression des Orotidin-5'-Decarboxylase-Gens pyrG steigert die Zitronensäureproduktion: eine neue Entdeckung beim recycelbaren Genome Editing in Aspergillus niger. | Zhang, L., et al. 2020. Microb Cell Fact. 19: 76. PMID: 32209089
- Orotidin-5'-Monophosphat-Decarboxylase: Die Funktionsweise von Active Site Chains innerhalb und zwischen den Proteinuntereinheiten. | Brandão, TAS. and Richard, JP. 2020. Biochemistry. 59: 2032-2040. PMID: 32374983
- Protein-Ribofuranosyl-Wechselwirkungen aktivieren die Orotidin-5'-Monophosphat-Decarboxylase zur Katalyse. | Cristobal, JR., et al. 2021. Biochemistry. 60: 3362-3373. PMID: 34726391
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Orotidine, 1 mg | sc-222103 | 1 mg | $173.00 | |||
Orotidine, 5 mg | sc-222103A | 5 mg | $675.00 | |||
Orotidine, 10 mg | sc-222103B | 10 mg | $1363.00 | |||
Orotidine, 25 mg | sc-222103C | 25 mg | $2965.00 |
