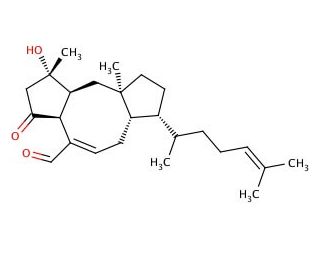
Ophiobolin C (CAS 19022-51-6)
Direktverknüpfungen
Ophiobolin C ist ein phytotoxischer Metabolit aus der Ophiobolin-Klasse, der von vielen Arten des Gattungs Bipolaris produziert wird. Studien deuten darauf hin, dass Ophiobolin C die Bindung von CCR5 an das Envelop-Protein gp120 und CD4 hemmt, was für die Mediation des Eintritts von HIV-1 in Zellen verantwortlich ist. Darüber hinaus ist das Kulturmedium ein wesentlicher Bestandteil für die Produktion eines bestimmten Ophiobolins aus demselben Organismus. Es wurde berichtet, dass B. maydis Ophiobolin A (sc-202266), B (sc-202267) und L in flüssigem Medium produzieren wird, während es im Gegensatz dazu Ophiobolin C und K in festem Substratmedium produziert. Die Struktur von Ophiobolin C besteht aus fünf Isopren-Einheiten, die zusammen die Rückgratmolekül bilden.
Ophiobolin C (CAS 19022-51-6) Literaturhinweise
- Die Biologie der Ophioboline. | Au, TK., et al. 2000. Life Sci. 67: 733-42. PMID: 10968403
- Isolierung und Struktur von Antagonisten des Chemokinrezeptors (CCR5). | Jayasuriya, H., et al. 2004. J Nat Prod. 67: 1036-8. PMID: 15217290
- Phytotoxine aus den pathogenen Pilzen Drechslera maydis und Drechslera sorghicola. | Sugawara, F., et al. 1987. Proc Natl Acad Sci U S A. 84: 3081-5. PMID: 16593832
- Strategien für die Synthese von Fusicoccanen durch Nazarov-Reaktionen von Dolabelladienonen: Totalsynthese von (+)-Fusicoauriton. | Williams, DR., et al. 2007. Angew Chem Int Ed Engl. 46: 915-8. PMID: 17171749
- Krebsstammzellenmedikamente zielen auf die K-ras-Signalübertragung in einem Stammzellenkontext ab. | Najumudeen, AK., et al. 2016. Oncogene. 35: 5248-5262. PMID: 26973241
- Multiple oxidative Modifikationen in der Ophiobolin-Biosynthese: P450-Oxidationen im Genom-Mining gefunden. | Narita, K., et al. 2016. Org Lett. 18: 1980-3. PMID: 27116000
- Die Biosynthese und der Transport von Ophiobolinen in Aspergillus ustus 094102. | Yan, J., et al. 2022. Int J Mol Sci. 23: PMID: 35163826
- Ophiobolin M und Analoga, nichtkompetitive Ivermectin-Bindungsinhibitoren mit nematozider Wirkung. | Tsipouras, A., et al. 1996. Bioorg Med Chem. 4: 531-6. PMID: 8735840
- Die unglaubliche Pilzgattung Drechslera - und ihre phytotoxischen Ophioboline | , et al. (1988). Phytoparasitica volume 16, pages 145–152 (1988). volume 16,: pages 145–152.
- Synthetische Studien zu natürlich vorkommenden Cyclooctanoiden. 1. Eine vollständige Synthese von (.+-.)-Ceroplastol I. | Robert K. Boeckman Jr., Argyrios Arvanitis, and Matthew E. Voss. 1989,. J. Am. Chem. Soc. 111, 7,: 2737–2739.
- Variecolin, ein Sesterterpenoid mit neuem Gerüst aus Aspergillus variecolor MF138 | Otto D. Hensens, Debra Zink, Joanne M. Williamson, Victor J. Lotti, Raymond S. L. Chang, and Michael A. Goetz. 1991. J. Org. Chem. 1991, 56, 10, 3399–3403., 56, 10,: 3399–3403.
- Ni(II)/Cr(II)-vermittelte Kupplungsreaktion: Günstige Auswirkungen von 4-tert-Butylpyridin als Additiv und Entwicklung neuer und verbesserter Aufarbeitungsverfahren | DP Stamos, XC Sheng, SS Chen, Y Kishi. September 1997,. Tetrahedron Letters. Volume 38, Issue 36, 8: Pages 6355-6358.
- Zytotoxische Sesterterpene, 6-epi-ophiobolin G und 6-epi-ophiobolin N, aus dem Meerespilz Emericella variecolor GF10 | H Wei, T Itoh, M Kinoshita, Y Nakai, M Kurotaki. 5 July 2004. Tetrahedron. Volume 60, Issue 28,,: Pages 6015-6019.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Ophiobolin C, 1 mg | sc-202268 | 1 mg | $300.00 |
