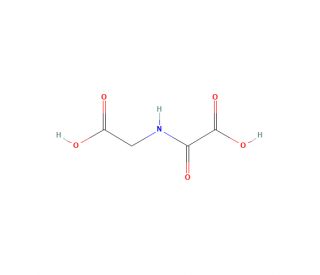
N-Oxalylglycine (CAS 5262-39-5)
Produktreferenzen ansehen (5)
Direktverknüpfungen
N-Oxalylglycin ist eine Verbindung, die als kompetitiver Inhibitor von 2-Oxoglutarat-abhängigen Dioxygenasen wirkt. Sie wirkt, indem sie das Eisen im aktiven Zentrum chelatiert und dadurch die Bindung des Co-Substrats verhindert und die enzymatische Aktivität hemmt. Der Wirkmechanismus von N-Oxalylglycin besteht in der Unterbrechung des katalytischen Zyklus von 2-Oxoglutarat-abhängigen Dioxygenasen, die an verschiedenen biologischen Prozessen wie der DNA- und Histon-Demethylierung sowie an hypoxischen Reaktionswegen beteiligt sind. Durch die Beeinträchtigung der enzymatischen Aktivität dieser Dioxygenasen kann N-Oxalylglycin dazu verwendet werden, die spezifische Rolle dieser Enzyme bei zellulären Prozessen und Signalwegen zu untersuchen. Seine Fähigkeit, das Eisen im aktiven Zentrum kompetitiv zu hemmen, kann für die Untersuchung der molekularen Mechanismen nützlich sein, die den Funktionen von 2-Oxoglutarat-abhängigen Dioxygenasen in verschiedenen experimentellen Anwendungen zugrunde liegen.
N-Oxalylglycine (CAS 5262-39-5) Literaturhinweise
- Kinetische und spektroskopische Untersuchung der Hemmung der FeII/alpha-Ketoglutarat-Dioxygenase, TauD, durch CoII, NiII und N-Oxalylglycin. | Kalliri, E., et al. 2005. Biochem Biophys Res Commun. 338: 191-7. PMID: 16165092
- Synthese und Aktivität von N-Oxalylglycin und seinen Derivaten als Jumonji C-Domäne enthaltende Histon-Lysin-Demethylase-Inhibitoren. | Hamada, S., et al. 2009. Bioorg Med Chem Lett. 19: 2852-5. PMID: 19359167
- Beweise für das Fehlen einer direkten transkriptionellen Unterdrückung des eisenregulierenden Peptids Hepcidin durch Hypoxie-induzierbare Faktoren. | Volke, M., et al. 2009. PLoS One. 4: e7875. PMID: 19924283
- Kraftfelddesign und Molekulardynamiksimulationen des Faktors, der HIF-1 hemmt, und seines Komplexes mit bekannten Inhibitoren: Implikationen für das rationale Design von Inhibitoren. | Park, H., et al. 2010. J Mol Graph Model. 29: 221-8. PMID: 20663694
- Der Breitspektrum-Inhibitor der 2-Oxoglutarat-Oxygenase N-Oxalylglycin ist in Rhabarber und Spinatblättern enthalten. | Al-Qahtani, K., et al. 2015. Phytochemistry. 117: 456-461. PMID: 26196940
- Neuartige markierungsfreie elektrochemische Strategie zur empfindlichen Bestimmung von Ten-Eleven-Translokationsprotein 1. | Yu, Z., et al. 2021. Anal Chim Acta. 1146: 140-145. PMID: 33461709
- Eine neue Reihe mutmaßlicher Histon-Demethylase-Inhibitoren für Brugia malayi als potenzielle Medikamente gegen Pilzerkrankungen. | Kreiss, T., et al. 2022. PLoS Negl Trop Dis. 16: e0010216. PMID: 35294431
- Konservierung der ungewöhnlichen dimeren JmjC-Faltung von JMJD7 von Drosophila melanogaster zum Menschen. | Chowdhury, R., et al. 2022. Sci Rep. 12: 6065. PMID: 35410347
- Korrektur des Herausgebers: MOG-Analoga zur Erforschung des MCT2-Pharmakophores, der α-Ketoglutarat-Biologie und der zellulären Auswirkungen von N-Oxalylglycin. | Fets, L., et al. 2022. Commun Biol. 5: 1019. PMID: 36167803
- Strukturanalyse der 2-Oxoglutarat-Bindungsstelle der mit dem zirkadianen Rhythmus verbundenen Oxygenase JMJD5. | Islam, MS., et al. 2022. Sci Rep. 12: 20680. PMID: 36450832
- Ein Hochdurchsatz-Effektor-Screening identifiziert ein neuartiges kleines Molekülgerüst zur Hemmung der Ten-Eleven-Translokationsdioxygenase 2. | Palei, S., et al. 2022. RSC Med Chem. 13: 1540-1548. PMID: 36545435
- Formaldehyd reagiert mit den N-terminalen Prolinresten zu bicyclischen Aminogruppen. | John, T., et al. 2023. Commun Chem. 6: 12. PMID: 36698022
- Substratselektivität und Hemmung der Histidin-JmjC-Hydroxylasen MINA53 und NO66. | Türkmen, VA., et al. 2023. RSC Chem Biol. 4: 235-243. PMID: 36908702
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
N-Oxalylglycine, 10 mg | sc-202720 | 10 mg | $53.00 | |||
N-Oxalylglycine, 100 mg | sc-202720A | 100 mg | $153.00 |
