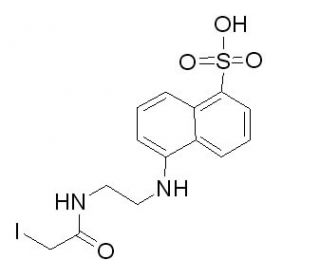
N-(Iodoacetaminoethyl)-1-naphthylamine-5-sulfonic acid (CAS 36930-63-9)
Direktverknüpfungen
N-(Iodacetaminoethyl)-1-naphthylamin-5-sulfonsäure ist ein fluoreszierendes Sulfhydrylreagenz, das sowohl in organischen Lösungsmitteln als auch in wässriger Lösung empfindlich auf photokatalytischen Abbau reagiert. Es reagiert leicht sowohl mit Sulfhydrylgruppen als auch mit Thiolverbindungen unter Bildung photostabiler kovalenter Derivate. Die Iodacetamidgruppe in N-(Iodacetaminoethyl)-1-naphthylamin-5-sulfonsäure ist unter physiologischen Bedingungen reaktiv gegenüber Cysteinthiolgruppen und ermöglicht die kovalente Modifikation von Proteinen. Diese selektive Reaktivität macht sie nützlich für die Markierung von Cysteinresten in Proteinen, die zur Untersuchung von Konformationsänderungen, Wechselwirkungen und Dynamik von Proteinen verwendet werden können.
N-(Iodoacetaminoethyl)-1-naphthylamine-5-sulfonic acid (CAS 36930-63-9) Literaturhinweise
- Streptolysin O: Die Hemmung der Konformationsänderung während der Membranbindung des Monomers verhindert Oligomerisierung und Porenbildung. | Abdel Ghani, EM., et al. 1999. Biochemistry. 38: 15204-11. PMID: 10563803
- Mechanistische Einblicke in die Spezifität, Aktivität und regulatorischen Elemente der Rho-spezifischen Guanin-Nukleotid-Austauschfaktoren (GEFs) p115, PDZ-RhoGEF (PRG) und Leukämie-assoziierter RhoGEF (LARG), die den Regulator der G-Protein-Signalübertragung (RGS) enthalten. | Jaiswal, M., et al. 2011. J Biol Chem. 286: 18202-12. PMID: 21454492
- Erzwungene Ausdehnung des Zytoskeletts delipidierter roter Blutkörperchen mit wenig Anzeichen für die Entfaltung von Spectrin. | Afrin, R., et al. 2012. Cytoskeleton (Hoboken). 69: 101-12. PMID: 22213694
- Biosynthese von 4-Thiouridin in tRNA in dem methanogenen Archaeon Methanococcus maripaludis. | Liu, Y., et al. 2012. J Biol Chem. 287: 36683-92. PMID: 22904325
- Studien zur subzellulären Fraktionierung und Lokalisierung zeigen eine direkte Interaktion des Fragile X Mental Retardation Protein (FMRP) mit Nucleolin. | Taha, MS., et al. 2014. PLoS One. 9: e91465. PMID: 24658146
- Persulfide: Aktuelles Wissen und Herausforderungen in Chemie und chemischer Biologie. | Park, CM., et al. 2015. Mol Biosyst. 11: 1775-85. PMID: 25969163
- De novo-Design von Protein-Protein-Wechselwirkungen durch Modifizierung von intermolekularen Helix-Helix-Schnittstellenresten. | Yagi, S., et al. 2016. Biochim Biophys Acta. 1864: 479-87. PMID: 26867971
- Defekte im mitochondrialen Aufbau von Eisen-Schwefel-Clustern induzieren Cystein-S-Polythiolierung auf Eisen-Schwefel-Apoproteinen. | Christ, S., et al. 2016. Antioxid Redox Signal. 25: 28-40. PMID: 26975213
- Die Wirkung von Maus-Twinfilin-1 auf die Struktur und Dynamik von monomerem Aktin. | Takács-Kollár, V., et al. 2016. Biochim Biophys Acta. 1864: 840-6. PMID: 27079635
- Spektroskopische Charakterisierung der Wirkung von Maus-Twinfilin-1 auf Aktinfilamente bei verschiedenen pH-Werten. | Takács-Kollár, V., et al. 2016. J Photochem Photobiol B. 164: 276-282. PMID: 27718419
- Strukturelle Auswirkungen der Phosphorylierung und der Variation der Dielektrizitätskonstante auf die IDR von Synaptotagmin. | Fealey, ME., et al. 2018. Biophys J. 114: 550-561. PMID: 29414700
- Crowder-induzierte strukturelle Modulation eines Multidomänen-Proteins während seiner frühen Aggregationsstadien: Eine FRET-basierte und Protein-Solvationsstudie. | Karmakar, S., et al. 2019. Int J Biol Macromol. 127: 563-574. PMID: 30658147
- Mechanismus des Zusammenbaus der oligomeren Streptolysin-O-Pore: Die frühe Membranläsion wird von einem freien Rand der Lipidmembran ausgekleidet und während der Oligomerisierung schrittweise erweitert. | Palmer, M., et al. 1998. EMBO J. 17: 1598-605. PMID: 9501081
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
N-(Iodoacetaminoethyl)-1-naphthylamine-5-sulfonic acid, 1 g | sc-218970 | 1 g | $426.00 |
