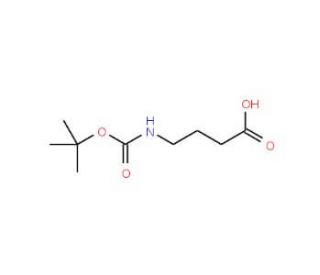
N-Boc-γ-aminobutyric acid (CAS 57294-38-9)
Direktverknüpfungen
N-Boc-γ-Aminobuttersäure fungiert als Schutzgruppe für den γ-Aminobuttersäure (GABA)-Teil. Sie wird in der Peptidsynthese zum Schutz der Aminogruppe von GABA verwendet und ermöglicht die selektive Manipulation anderer funktioneller Gruppen. Die N-Boc-Gruppe wird in der Regel unter milden sauren Bedingungen entfernt, was die Synthese von GABA-haltigen Peptiden ermöglicht. Der Wirkungsmechanismus von N-Boc-γ-Aminobuttersäure beinhaltet den reversiblen Schutz der Aminogruppe, wodurch unerwünschte Reaktionen während der Peptidsynthese verhindert werden. Indem sie als Schutzgruppe dient, erleichtert N-Boc-γ-Aminobuttersäure die kontrollierte Modifizierung von GABA-haltigen Peptiden und trägt so zur Synthese komplexer Peptidstrukturen bei. Ihre Rolle in der Peptidsynthese besteht in der präzisen Manipulation funktioneller Gruppen, die die Schaffung verschiedener Peptidsequenzen ohne Beeinträchtigung des GABA-Anteils ermöglicht.
N-Boc-γ-aminobutyric acid (CAS 57294-38-9) Literaturhinweise
- Inibitori della farnesiltransferasi bisubstrato non peptidici e non prerenilici. Parte 3: requisiti strutturali della parte centrale per l'attività inibitoria della farnesiltransferasi. | Schlitzer, M., et al. 2000. Bioorg Med Chem. 8: 2399-406. PMID: 11058034
- Farnesyltransferase-Inhibitoren, die keine Thiole sind: Struktur-Wirkungs-Beziehungen von Farnesyltransferase-Inhibitoren auf Benzophenon-Basis mit Bisubstrat-Analoga. | Schlitzer, M., et al. 2002. Bioorg Med Chem. 10: 615-20. PMID: 11814849
- Fluorierte photoremovable Schutzgruppen: der Einfluss von Fluorsubstituenten auf die Photo-Favorskii-Umlagerung. | Stensrud, KF., et al. 2008. Photochem Photobiol Sci. 7: 614-24. PMID: 18465018
- Synthese und Bewertung der antibakteriellen Aktivität von Metronidazol-Triazol-Konjugaten. | Beena, ., et al. 2009. Bioorg Med Chem Lett. 19: 1396-8. PMID: 19195884
- p-Hydroxyphenacyl photoremovable Schutzgruppen - Robuste Photochemie trotz Substituentenvielfalt. | Givens, RS., et al. 2011. Can J Chem. 89: 364-384. PMID: 24436496
- Inhibitoren der bicyclisch-verkappten Histon-Deacetylase 6 mit verbesserter Aktivität in einem Modell der axonalen Charcot-Marie-Tooth-Krankheit. | Shen, S., et al. 2016. ACS Chem Neurosci. 7: 240-58. PMID: 26599234
- Zelluläre Aktivität von neuen niedermolekularen Protein Arginin Deiminase 3 (PAD3) Inhibitoren. | Jamali, H., et al. 2016. ACS Med Chem Lett. 7: 847-51. PMID: 27660689
- Entwicklung einer selektiven Mono- oder Dual-PROTAC-Degradatorsonde für CDK-Isoformen. | Zhou, F., et al. 2020. Eur J Med Chem. 187: 111952. PMID: 31846828
- Entdeckung eines d-Pro-Lys-Peptidomimetikums als Inhibitor von MMP9: Untersuchung der Selektivität der Gelatinase über den S1'-Teilbereich hinaus | Lenci, E., et al. 2020. Bioorg Med Chem Lett. 30: 127467. PMID: 32768649
- Neue Benzoxazole mit 4-Amino-Butanamid-Anteil hemmten LPS-induzierte Entzündungen durch Modulierung der IL-6- oder IL-1β-mRNA-Expression. | Yoo, J., et al. 2022. Int J Mol Sci. 23: PMID: 35628136
- Folsäurefunktionalisierung für zielgerichtete selbstorganisierte Nanopartikel auf Paclitaxelbasis. | Colombo, E., et al. 2022. RSC Adv. 12: 35484-35493. PMID: 36544466
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
N-Boc-γ-aminobutyric acid, 1 g | sc-279719 | 1 g | $49.00 |
