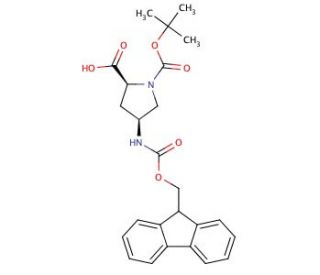
N-Boc-cis-4-N-Fmoc-amino-L-proline (CAS 174148-03-9)
Direktverknüpfungen
N-Boc-cis-4-N-Fmoc-amino-L-Prolin ist eine chemisch geschützte Form der Aminosäure Prolin, die speziell für die Peptidsynthese entwickelt wurde. Diese Verbindung weist zwei Schutzgruppen auf: die tert-Butoxycarbonylgruppe (Boc) und die Fluorenylmethyloxycarbonylgruppe (Fmoc). Die Boc-Gruppe schützt die Aminfunktionalität, während die Fmoc-Gruppe an das Stickstoffatom des Prolinrings gebunden ist und den Amidstickstoff schützt. Diese Schutzgruppen sind für die Peptidsynthese mit Festphasentechniken von entscheidender Bedeutung, da sie unerwünschte Nebenreaktionen verhindern und den korrekten Aufbau der Peptidsequenz gewährleisten. Die cis-Konfiguration des Prolinrestes in N-Boc-cis-4-N-Fmoc-amino-L-Prolin ist besonders wichtig, da die cis- und trans-Isomere von Prolin die Faltung und Funktion von Peptiden und Proteinen erheblich beeinflussen können. In der Forschung wird diese Spezifität ausgenutzt, um die strukturelle Dynamik von Peptiden und die Rolle der Prolin-Isomerisierung bei biologischen Prozessen zu untersuchen. N-Boc-cis-4-N-Fmoc-amino-L-Prolin ermöglicht es den Wissenschaftlern, den Einbau von cis-Prolin in Peptide genau zu kontrollieren, was Untersuchungen darüber erleichtert, wie die Konformation von Prolin die Peptidstruktur, die Stabilität und die Interaktion mit anderen Molekülen beeinflusst. Solche Studien sind in der Biochemie und Molekularbiologie von grundlegender Bedeutung, da sie Einblicke in die Mechanismen der Proteinfaltung und den Entwurf neuartiger Peptide für wissenschaftliche Experimente ermöglichen, wobei therapeutische oder klinische Anwendungen ausgeschlossen sind.
N-Boc-cis-4-N-Fmoc-amino-L-proline (CAS 174148-03-9) Literaturhinweise
- Entwicklung einer anpassbaren Plattform für Fluoreszenzsonden zum Nachweis bioaktiver Spezies, die auf Organellen ausgerichtet sind. | Qiao, D., et al. 2020. ACS Sens. 5: 2247-2254. PMID: 32627537
- Neue, potente, niedermolekulare Agonisten von Tyrosinkinase-Rezeptoren lindern die Krankheit des trockenen Auges. | Yu, Z., et al. 2022. Front Med (Lausanne). 9: 937142. PMID: 36091713
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
N-Boc-cis-4-N-Fmoc-amino-L-proline, 1 g | sc-391067 | 1 g | $153.00 |
