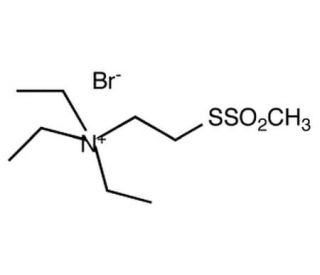
MTS-TEAE
Direktverknüpfungen
MTS-TEAE, ein wasserlösliches, größer strukturiertes Analogon des geladenen MTS-Reagenzes MTSET, wird häufig in der biochemischen Forschung verwendet. Geladene MTS-Reagenzien wurden erfolgreich mit der SCAM-Methode (Substituted Cysteine Accessibility Method) eingesetzt, um die Topologie und Funktion einer Reihe von ligandengesteuerten Ionenkanälen und Transporterproteinen zu untersuchen. MTS-TEAE, auch bekannt als (2-(Trimethylammonium)ethyl) Methanthiosulfonat, wird in Studien zur Bioconjugation und Proteinmodifikation verwendet. Es handelt sich um ein sulfhydrylreaktives Reagenz, das selektiv mit Cysteinresten in Proteinen reagiert und eine kovalente Bindung bildet.MTS-TEAE wird oft in Techniken der ortsgerichteten Mutagenese und Protein-Engineering eingesetzt, um spezifische Modifikationen oder Sonden an Cysteinresten einzuführen. Durch seine Fähigkeit, gezielt mit Cysteinresten zu reagieren, ermöglicht es die präzise Modifikation von Proteinstrukturen, was für das Verständnis ihrer Funktion und Struktur entscheidend ist. Dies macht MTS-TEAE zu einem wichtigen Werkzeug in der biologischen und biomedizinischen Forschung, insbesondere in Studien zur Proteinstruktur und -funktion.
MTS-TEAE Literaturhinweise
- Strukturelle Determinanten der Ionenpermeation in CRAC-Kanälen. | McNally, BA., et al. 2009. Proc Natl Acad Sci U S A. 106: 22516-21. PMID: 20018736
- Beteiligung der Transmembrandomäne 1 von Presenilin 1 an der katalytischen Porenstruktur der γ-Sekretase. | Takagi, S., et al. 2010. J Neurosci. 30: 15943-50. PMID: 21106832
- Kooperative Rolle der hydrophilen Schleife 1 und des C-Terminus von Presenilin 1 im Substrat-Gating-Mechanismus der γ-Sekretase. | Takagi-Niidome, S., et al. 2015. J Neurosci. 35: 2646-56. PMID: 25673856
- Der STIM-Orai-Weg: Orai, die porenbildende Untereinheit des CRAC-Kanals. | Gudlur, A. and Hogan, PG. 2017. Adv Exp Med Biol. 993: 39-57. PMID: 28900908
- Die Konformationsdynamik der Transmembrandomäne 3 von Presenilin 1 ist mit der Trimmaktivität der γ-Sekretase verbunden. | Cai, T., et al. 2019. J Neurosci. 39: 8600-8610. PMID: 31527118
- Untersuchung von Permeation und Gating von Orai-Kanälen durch chemische Modifikation von Cysteinresten. | Yamashita, M. and Prakriya, M. 2021. Methods Enzymol. 652: 213-239. PMID: 34059283
- Strukturanalyse des Zielproteins durch die Methode der Zugänglichkeit von substituiertem Cystein. | Cai, T. and Tomita, T. 2018. Bio Protoc. 8: e2470. PMID: 34395783
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
MTS-TEAE, 10 mg | sc-215395 | 10 mg | $379.00 |
