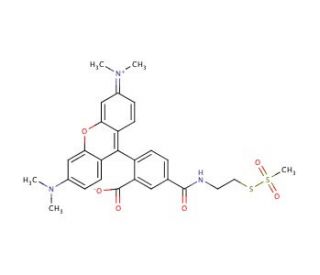
Molekülstruktur von MTS-TAMRA, CAS-Nummer: 1329837-19-5
MTS-TAMRA (CAS 1329837-19-5)
Produktreferenzen ansehen (4)
Alternative Namen:
MTS-TAMRA is known as a Sulfhydryl-active fluorescent reagent.
Anwendungen:
MTS-TAMRA ist eine sulfhydrylselektive fluoreszierende Verbindung, die zur schnellen, selektiven Modifizierung von Sulfhydryl-Enzymen verwendet wird.
CAS Nummer:
1329837-19-5
Molekulargewicht:
567.68
Summenformel:
C28H29N3O6S2
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Publikationen
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
MTS-TAMRA ist ein fluoreszierendes Molekül, das zur schnellen und selektiven Modifizierung von Sulfhydrylgruppen von Enzymen verwendet wird. Es gibt ein Fluoreszenzmaximum bei 535nm in MTS-TAMRA. Es gibt auch ein Fluoreszenzmaximum bei 605nm in MTS-TAMRA.
MTS-TAMRA (CAS 1329837-19-5) Literaturhinweise
- NBCe1-A Transmembransegment 1 leitet den Ionen-Translokationsweg ein. | Zhu, Q., et al. 2009. J Biol Chem. 284: 8918-29. PMID: 19158093
- Ligandenspezifische Konformationsänderungen in der ligandenbindenden Domäne des Alpha1-Glycinrezeptors. | Pless, SA. and Lynch, JW. 2009. J Biol Chem. 284: 15847-56. PMID: 19286654
- Substrat-Interaktionen des elektroneutralen Na+-gekoppelten anorganischen Phosphat-Cotransporters (NaPi-IIc). | Ghezzi, C., et al. 2009. J Physiol. 587: 4293-307. PMID: 19596895
- Topologische Lage und strukturelle Bedeutung der bei der proximalen renalen tubulären Azidose mutierten NBCe1-A-Reste. | Zhu, Q., et al. 2010. J Biol Chem. 285: 13416-26. PMID: 20197274
- Die relative Ausrichtung der TM3- und TM4-Domänen variiert zwischen α1- und α3-Glycinrezeptoren. | Han, L., et al. 2013. ACS Chem Neurosci. 4: 248-54. PMID: 23421675
- Korrelation von Ladungsbewegungen mit lokalen Konformationsänderungen eines Na(+)-gekoppelten Cotransporters. | Patti, M. and Forster, IC. 2014. Biophys J. 106: 1618-29. PMID: 24739161
- Die Kinetik von Konformationsänderungen, die mit Hilfe der Spannungsklemmen-Fluorometrie ermittelt wurden, geben Aufschluss über die Desensibilisierung an ATP-gesteuerten menschlichen P2X1-Rezeptoren. | Fryatt, AG. and Evans, RJ. 2014. Mol Pharmacol. 86: 707-15. PMID: 25296688
- Mechanistische Erkenntnisse aus der Aufklärung der ligandenabhängigen Kinetik von Konformationsänderungen an ATP-gesteuerten P2X1R-Ionenkanälen. | Fryatt, AG., et al. 2016. Sci Rep. 6: 32918. PMID: 27616669
- Strukturelle und funktionelle Bedeutung der Wasserpermeation durch Cotransporter. | Zeuthen, T., et al. 2016. Proc Natl Acad Sci U S A. 113: E6887-E6894. PMID: 27791155
- Active Site Voltage Clamp Fluorometrie des Natrium-Glukose-Cotransporters hSGLT1. | Gorraitz, E., et al. 2017. Proc Natl Acad Sci U S A. 114: E9980-E9988. PMID: 29087341
- Hochempfindliche Fluorometrie zur Auflösung der Konformationsdynamik von Ionenkanälen. | Wulf, M. and Pless, SA. 2018. Cell Rep. 22: 1615-1626. PMID: 29425514
- Die Kartierung der Bindungsstelle des P2X-Rezeptorantagonisten PPADS zeigt die Bedeutung der orthosterischen Ladung der Stelle und der cysteinreichen Kopfregion. | Huo, H., et al. 2018. J Biol Chem. 293: 12820-12831. PMID: 29997254
- Erhellung eines progressiven allosterischen Mechanismus, der die Aktivierung des Glycinrezeptors vermittelt. | Shi, S., et al. 2023. Nat Commun. 14: 795. PMID: 36781912
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
MTS-TAMRA, 1 mg | sc-215393 | 1 mg | $320.00 | |||
MTS-TAMRA, 10 mg | sc-215393A | 10 mg | $2200.00 |
