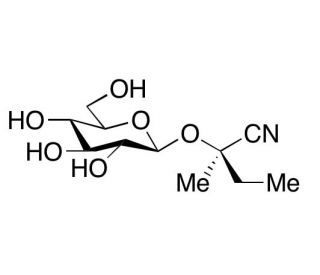
Molekülstruktur von Lotaustralin, CAS-Nummer: 534-67-8
Lotaustralin (CAS 534-67-8)
Produktreferenzen ansehen (2)
Alternative Namen:
(R)-2-(β-D-Glucopyranosyloxy)-2-methylbutyronitrile; (2R)-2-(β-D-Glucopyranosyloxy)-2-methyl-butanenitrile
Anwendungen:
Lotaustralin ist ein Kohlenhydratderivat
CAS Nummer:
534-67-8
Molekulargewicht:
261.27
Summenformel:
C11H19NO6
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Publikationen
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
Lotaustralin ist ein cyanogener Glucosid, der in geringen Mengen in einer Vielzahl von Pflanzen vorkommt. Lotaustralin ist das Glucosid von Methyl-Ethyl-Keton-Cyanhydrin und ist strukturell mit Linamarin verbunden, einem Aceton-Cyanhydrin-Glucosid, das ebenfalls in Pflanzen vorkommt. Sowohl Lotaustralin als auch Linamarin können durch das Enzym Linamarase hydrolysiert werden, um Glucose und einen Vorstufe des toxischen Stoffes Hydrogencyanid zu bilden.
Lotaustralin (CAS 534-67-8) Literaturhinweise
- [Quantitative Analyse von Salidrosid und Lotaustralin in Rhodiola durch Gaschromatographie]. | Kang, S., et al. 1998. Zhongguo Zhong Yao Za Zhi. 23: 365-6, 384. PMID: 11601302
- Biosynthese der Nitrilglucoside Rhodiocyanosid A und D sowie der cyanogenen Glucoside Lotaustralin und Linamarin in Lotus japonicus. | Forslund, K., et al. 2004. Plant Physiol. 135: 71-84. PMID: 15122013
- Muster des Cyanid-Potentials in sich entwickelnden Früchten: Implikationen für Pflanzen, die cyanogene Monoglucoside (Phaseolus lunatus) oder cyanogene Diglucoside in ihren Samen anreichern (Linum usitatissimum, Prunus amygdalus). | Frehner, M., et al. 1990. Plant Physiol. 94: 28-34. PMID: 16667698
- Die Zusammensetzung der cyanogenen Glucoside von Zygaena filipendulae (Lepidoptera: Zygaenidae) durch Fütterung von Wildtyp- und transgenen Lotuspopulationen mit unterschiedlichen cyanogenen Glucosidprofilen. | Zagrobelny, M., et al. 2007. Insect Biochem Mol Biol. 37: 10-8. PMID: 17175442
- Cyanogene Glykoside in Schmetterlingen: Nachweis und Synthese von Linamarin und Lotaustralin bei den Helikoniern. | Nahrstedt, A. and Davis, RH. 1981. Planta Med. 42: 124-5. PMID: 17401921
- Auswirkungen der Wirtspflanze Linamarin und Lotaustralin auf Tetranychus urticae und seinen Räuber Phytoseiulus persimilis auf tri-tropischer Ebene. | Rojas, MG. and Morales-Ramos, JA. 2010. J Chem Ecol. 36: 1354-62. PMID: 20953678
- Biosynthese der cyanogenen Glucoside Linamarin und Lotaustralin in Maniok: Isolierung, biochemische Charakterisierung und Expressionsmuster von CYP71E7, dem oxim-metabolisierenden Cytochrom-P450-Enzym. | Jørgensen, K., et al. 2011. Plant Physiol. 155: 282-92. PMID: 21045121
- Bestimmung von cyanogenen Glucosiden in Trifolium-Arten mittels Ultra-Performance-Flüssigkeitschromatographie und Tandem-Massenspektrometrie. | Muzashvili, T., et al. 2014. J Agric Food Chem. 62: 1777-82. PMID: 24476020
- Das evolutionäre Auftreten von nicht-cyanogenen Hydroxynitril-Glucosiden in der Lotus-Gattung wird von der Substratspezialisierung paraloger β-Glucosidasen begleitet, die aus einer entscheidenden Aminosäuresubstitution resultiert. | Lai, D., et al. 2014. Plant J. 79: 299-311. PMID: 24861854
- Biosynthese von cyanogenen Glucosiden in Phaseolus lunatus und die Entwicklung der oximbasierten Abwehrkräfte. | Lai, D., et al. 2020. Plant Direct. 4: e00244. PMID: 32775954
- Eigenschaften eines mikrosomalen Enzymsystems aus Linum usitatissimum (Lein Lein), das Valin zu Acetoncyanohydrin und Isoleucin zu 2-Methylbutanoncyanohydrin oxidiert. | Cutler, AJ., et al. 1985. Arch Biochem Biophys. 238: 272-9. PMID: 3985623
- Cyanogene und nicht-cyanogene Glykoside aus Manihot esculenta. | Prawat, H., et al. 1995. Phytochemistry. 40: 1167-73. PMID: 7492370
- Bioaktive Bestandteile der chinesischen Naturheilkunde. IV. Rhodiolae radix. (2).: Über die Histaminfreisetzungshemmer aus dem unterirdischen Teil von Rhodiola sacra (Prain ex Hamet) S. H. Fu (Crassulaceae): chemische Strukturen von Rhodiocyanosid D und Sacranoside A und B. | Yoshikawa, M., et al. 1997. Chem Pharm Bull (Tokyo). 45: 1498-503. PMID: 9332002
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Lotaustralin, 2.5 mg | sc-207835 | 2.5 mg | $634.00 | |||
Lotaustralin, 25 mg | sc-207835A | 25 mg | $3797.00 |
