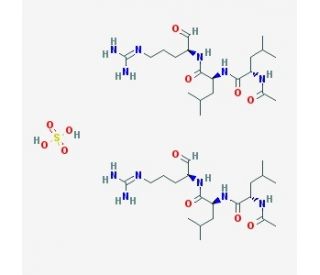
Leupeptin hemisulfate (CAS 103476-89-7)
Produktreferenzen ansehen (19)
Direktverknüpfungen
Leupeptinhemisulfat ist ein reversibler, kompetitiver Proteaseinhibitor, der Cathepsine B, H, L und S, Calpain und Trypsin hemmt. Es ist ein reversibler Inhibitor von Cystein-, Serin- und Threonin-Proteasen, die natürlicherweise von Streptomyces produziert werden. Leupeptinhemisulfat hat keine Wirkung gegen Chymotrypsin, Elastase, Renin oder Pepsin. In der biochemischen Forschung wird es häufig als Reduktionsmittel in Experimenten verwendet, die darauf abzielen, Proteine, Enzyme, Aminosäuren und Neuropeptide zu untersuchen. Leupeptinhemisulfat kann auch als Werkzeug zur Proteinreinigung verwendet werden, um Proteasen in Gewebeproben daran zu hindern, das Protein von Interesse abzubauen. Forscher verwenden es, um die Auswirkungen der Protease-Inhibition auf den Zellstoffwechsel, die Enzymaktivität, die Genexpression, die Proteinsynthese, den Proteinabbau und die Protein-Faltung zu untersuchen.
Leupeptin hemisulfate (CAS 103476-89-7) Literaturhinweise
- Charakterisierung der intrazellulären Komplexe der reversen Transkription des humanen Immundefizienzvirus Typ 1. | Fassati, A. and Goff, SP. 2001. J Virol. 75: 3626-35. PMID: 11264352
- Sequenzanalyse, Gewebeverteilung und Expression von Ratten-Cathepsin S. | Petanceska, S. and Devi, L. 1992. J Biol Chem. 267: 26038-43. PMID: 1281481
- Die Phosphorylierung der p70s6-Kinase ist am androgenbedingten Anabolismus des Levator-Ani-Muskels bei kastrierten Ratten beteiligt. | Xu, T., et al. 2004. J Steroid Biochem Mol Biol. 92: 447-54. PMID: 15698549
- Mikrotubuli in Mesophyllzellen von nicht akklimatisiertem und kälteakklimatisiertem Spinat: Visualisierung und Reaktionen auf Gefrieren, niedrige Temperaturen und Austrocknung. | Bartolo, ME. and Carter, JV. 1991. Plant Physiol. 97: 175-81. PMID: 16668366
- Inhibitoren von Cathepsin B. | Frlan, R. and Gobec, S. 2006. Curr Med Chem. 13: 2309-27. PMID: 16918357
- Charakterisierung vaskulär-spezifischer RSs1- und rolC-Promotoren im Hinblick auf ihre Verwendung bei der Pflanzenzüchtung zur Entwicklung von Resistenzen gegen hemipterische Insektenschädlinge. | Saha, P., et al. 2007. Planta. 226: 429-42. PMID: 17323077
- Analyse der Grenzen der Expression des Hepatitis-B-Oberflächenantigens in Sojabohnen-Zellsuspensionskulturen. | Ganapathi, TR., et al. 2007. Plant Cell Rep. 26: 1575-84. PMID: 17534624
- Isolierung von zytokinetischen Actomyosin-Ringen aus Saccharomyces cerevisiae und Schizosaccharomyces pombe. | Huang, J., et al. 2016. Methods Mol Biol. 1369: 125-136. PMID: 26519310
- Hemmung der proteolytischen Aktivitäten in Pflanzenzellen, die Tubulin abbauen. | Morejohn, LC., et al. 1985. Cell Biol Int Rep. 9: 849-57. PMID: 2864138
- Herstellung von Clathrin-ummantelten Vesikeln aus Arabidopsis thaliana-Sämlingen. | Mosesso, N., et al. 2018. Front Plant Sci. 9: 1972. PMID: 30687367
- Leupeptine, neue Proteaseinhibitoren aus Actinomycetes. | Aoyagi, T., et al. 1969. J Antibiot (Tokyo). 22: 283-6. PMID: 5810993
- Taxol-induzierte rosa Mikrotubuli-Polymerisation in vitro und ihre Hemmung durch Colchicin. | Morejohn, LC. and Fosket, DE. 1984. J Cell Biol. 99: 141-7. PMID: 6145718
- Cathepsin B, Cathepsin H und Cathepsin L. | Barrett, AJ. and Kirschke, H. 1981. Methods Enzymol. 80 Pt C: 535-61. PMID: 7043200
- Humanes Cathepsin B. Anwendung des Substrats N-Benzyloxycarbonyl-L-Arginyl-L-Arginin-2-Naphthylamid für eine Studie über die Hemmung durch Leupeptin. | Knight, CG. 1980. Biochem J. 189: 447-53. PMID: 7213339
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Leupeptin hemisulfate, 5 mg | sc-295358 | 5 mg | $72.00 | |||
Leupeptin hemisulfate, 10 mg | sc-295358C | 10 mg | $99.00 | |||
Leupeptin hemisulfate, 25 mg | sc-295358A | 25 mg | $145.00 | |||
Leupeptin hemisulfate, 50 mg | sc-295358D | 50 mg | $265.00 | |||
Leupeptin hemisulfate, 100 mg | sc-295358E | 100 mg | $489.00 | |||
Leupeptin hemisulfate, 500 mg | sc-295358B | 500 mg | $1399.00 |
