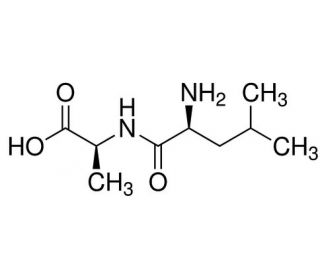
L-Leucyl-L-alanine (CAS 7298-84-2)
Direktverknüpfungen
L-Leucyl-L-Alanin ist ein Dipeptid, das die ubiquitinvermittelte Proteinabbau hemmen kann. Es wird als Fluoreszenzverstärker in fluorimetrischen Methoden zur Bestimmung von Phenylalanin verwendet. L-Leucyl-L-Alanin wurde in vitro untersucht, um seine Auswirkungen auf Zellkulturen zu verstehen, insbesondere seinen Effekt auf Zellwachstum und -differenzierung. Obwohl der Wirkungsmechanismus von L-Leucyl-L-Alanin nicht vollständig verstanden ist, wird vermutet, dass es als Substrat für Enzyme fungiert, die eine Rolle in der Proteinsynthese und im Energiestoffwechsel spielen. Darüber hinaus wird angenommen, dass es an der Regulation der Genexpression und der Zellsignalwege beteiligt ist. Forscher haben festgestellt, dass L-Leucyl-L-Alanin die Produktion von Zytokinen, einschließlich Interleukin-1β und Tumor-Nekrosefaktor-α, stimulieren kann, die für die Immunantwort essentiell sind. Darüber hinaus hat es antimikrobielle Eigenschaften gegen verschiedene Bakterien wie Escherichia coli, Staphylococcus aureus und Pseudomonas aeruginosa gezeigt. Die Verbindung wurde auch auf ihr Potenzial als entzündungshemmendes Mittel untersucht.
L-Leucyl-L-alanine (CAS 7298-84-2) Literaturhinweise
- Schätzung der genetischen Divergenz und Identifizierung von drei Trichinenarten durch Isoenzymanalyse. | Snábel, V., et al. 2001. Parasite. 8: S30-3. PMID: 11484377
- Auswirkungen der Kombination eines Proteasominhibitors (PSI) und eines Inhibitors von Ubiquitin-Ligasen (Leu-Ala) auf die Ultrastruktur von menschlichen leukämischen U937-Zellen. | Biały, LP., et al. 2002. Folia Histochem Cytobiol. 40: 135-6. PMID: 12056612
- Expression, Reinigung und Charakterisierung eines minimierten Hühner-Riboflavinträgerproteins aus einem synthetischen Gen in Escherichia coli. | Subramanian, S., et al. 2002. Protein Expr Purif. 26: 284-9. PMID: 12406683
- [Racemische Spaltung von Valyl-Glycin-, Leucyl-Glycin- und Alanyl-Beta-Alanin-Estern]. | LOSSE, G., et al. 1959. Hoppe Seylers Z Physiol Chem. 314: 224-33. PMID: 13664211
- Die Entwicklung von VIP-Elipticin-Konjugaten. | Moody, TW., et al. 2004. Regul Pept. 123: 187-92. PMID: 15518911
- Design, Synthese und Röntgenstruktur von potenten Memapsin 2 (beta-Sekretase) Inhibitoren mit Isophthalamid-Derivaten als P2-P3-Liganden. | Ghosh, AK., et al. 2007. J Med Chem. 50: 2399-407. PMID: 17432843
- Potente Memapsin 2 (Beta-Sekretase) Inhibitoren: Design, Synthese, Protein-Ligand Röntgenstruktur und in vivo Evaluierung. | Ghosh, AK., et al. 2008. Bioorg Med Chem Lett. 18: 1031-6. PMID: 18180160
- Konstruktion von kovalent gekoppelten, konkatameren Dimeren von 7TM-Rezeptoren. | Terpager, M., et al. 2009. J Recept Signal Transduct Res. 29: 235-45. PMID: 19747085
- Antimikrobielle Metaboliten aus einem neuartigen halophilen Aktinomyceten Nocardiopsis terrae YIM 90022. | Tian, S., et al. 2014. Nat Prod Res. 28: 344-6. PMID: 24236566
- Genetische Variation von Peptidase und Pyrophosphatase beim Huhn. | Lundin, LG. and Wilhelmson, M. 1989. Poult Sci. 68: 1313-8. PMID: 2555801
- Potente Komplement-C3a-Rezeptor-Agonisten auf der Basis von Oxazol-Aminosäuren: Struktur-Aktivitäts-Beziehungen. | Singh, R., et al. 2015. Bioorg Med Chem Lett. 25: 5604-8. PMID: 26522948
- Reinigung und Identifizierung entzündungshemmender Peptide, die aus simulierten gastrointestinalen Verdauungen von Samtgeweihprotein (Cervus elaphus Linnaeus) stammen. | Zhao, L., et al. 2016. J Food Drug Anal. 24: 376-384. PMID: 28911592
- Orte der Dipeptidhydrolyse im Verhältnis zu Orten des aktiven Histidin- und Glukosetransports im Hamsterdarm. | Wiseman, G. 1983. J Physiol. 342: 421-35. PMID: 6631743
- Isolierung und Strukturaufklärung von zwei neuen Calpain-Inhibitoren aus Streptomyces griseus. | Alvarez, ME., et al. 1994. J Antibiot (Tokyo). 47: 1195-201. PMID: 8002381
- Analyse von Aminopeptidase und Dipeptidylpeptidase IV aus dem entomopathogenen Pilz Metarhizium anisopliae. | St Leger, RJ., et al. 1993. J Gen Microbiol. 139: 237-43. PMID: 8094738
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
L-Leucyl-L-alanine, 1 g | sc-300885 | 1 g | $92.00 | |||
L-Leucyl-L-alanine, 5 g | sc-300885A | 5 g | $240.00 | |||
L-Leucyl-L-alanine, 25 g | sc-300885B | 25 g | $999.00 | |||
L-Leucyl-L-alanine, 100 g | sc-300885C | 100 g | $3937.00 |
