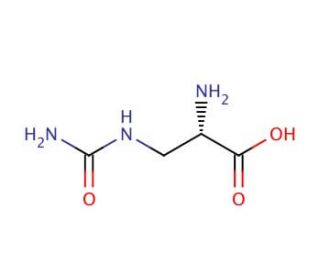
L-Albizziin (CAS 1483-07-4)
Direktverknüpfungen
L-Albizziin ist bekannt für seine Rolle als potenter Inhibitor der Glucosamin-6-Phosphat-Synthase, einem Enzym, das entscheidend an der Biosynthese von Aminozuckern beteiligt ist. Forscher nutzen diese Verbindung, um die Funktion und Regulation des Enzyms zu untersuchen, was für das Verständnis des Aminozuckerstoffwechsels und seiner Auswirkungen auf verschiedene biologische Prozesse entscheidend ist. Die Fähigkeit, dieses Enzym selektiv zu hemmen, macht es zu einem wertvollen Werkzeug zur Untersuchung der Stoffwechselwege, die zur Zellwandbiosynthese beitragen, insbesondere bei Pilzorganismen. Darüber hinaus wird L-Albizziin bei Untersuchungen eingesetzt, die darauf abzielen, die Mechanismen der Antibiotikaresistenz zu klären, die die Aminozuckerwege betreffen, und Einblicke zu gewinnen, die zu neuen Strategien zur Bekämpfung resistenter mikrobieller Arten führen könnten. Seine Anwendung in der Forschung erstreckt sich auch auf die Erforschung der Chitinproduktion, einem Bestandteil der Pilzzellwand.
L-Albizziin (CAS 1483-07-4) Literaturhinweise
- Reinigung und Charakterisierung einer neuen Cysteinkonjugat-Beta-Lyase aus dem Bandwurm Moniezia expansa. | Adcock, HJ., et al. 2000. Int J Parasitol. 30: 567-71. PMID: 10779568
- Molekulare Erkennung von Aminosäuren durch RNA-Aptamere: die Entwicklung eines Dopamin-bindenden RNA-Motivs zu einem L-Tyrosin-Binder. | Mannironi, C., et al. 2000. RNA. 6: 520-7. PMID: 10786843
- Reinigung und Charakterisierung einer Glutaminase aus Debaryomyces spp. | Durá, MA., et al. 2002. Int J Food Microbiol. 76: 117-26. PMID: 12038568
- Glutamin-Stoffwechsel in den Skelettmuskeln des Mastkükens (Gallus domesticus) und der Laborratte (Rattus norvegicus). | Wu, GY., et al. 1991. Biochem J. 274 (Pt 3): 769-74. PMID: 2012604
- Biochemische Charakterisierung und Antitumoruntersuchung von L-Glutaminase aus Bacillus cereus MTCC 1305. | Singh, P. and Banik, RM. 2013. Appl Biochem Biotechnol. 171: 522-31. PMID: 23873638
- Kynurenin-Aminotransferase III und Glutamin-Transaminase L sind identische Enzyme, die Cystein-S-Konjugat-β-Lyase-Aktivität besitzen und L-Selenomethionin transaminieren können. | Pinto, JT., et al. 2014. J Biol Chem. 289: 30950-61. PMID: 25231977
- Reinigung und Charakterisierung von Cysteinkonjugat-Transaminasen aus Rattenleber. | Tomisawa, H., et al. 1988. Xenobiotica. 18: 1015-28. PMID: 2852419
- Reinigung, Charakterisierung und krebshemmende Wirkung von L-Glutaminase aus Aspergillus flavus. | Abu-Tahon, MA. and Isaac, GS. 2020. J Gen Appl Microbiol. 65: 284-292. PMID: 31130583
- Identifizierung eines reaktiven Cysteinrestes an der Glutaminbindungsstelle der Carbamylphosphatsynthetase. | Pinkus, LM. and Meister, A. 1972. J Biol Chem. 247: 6119-27. PMID: 4568602
- Wirkung von Leber-Glutamin-Transaminase und L-Aminosäure-Oxidase auf verschiedene Glutamin-Analoga. Herstellung und Eigenschaften der 4-S-, O- und NH-Analoga der Alpha-Ketoglutaraminsäure. | Cooper, AJ. and Meister, A. 1973. J Biol Chem. 248: 8499-505. PMID: 4797019
- Hemmung von Homocysteinsulfonamid der aus Saccharomyces cerevisiae gereinigten Glutamatsynthase. | Masters, DS. and Meister, A. 1982. J Biol Chem. 257: 8711-5. PMID: 7047525
- [Metabolismus von L-Albizziin in Rattenleberscheiben]. | Fitsner, AB. 1978. Vopr Med Khim. 24: 832-6. PMID: 734988
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
L-Albizziin, 250 mg | sc-218627 | 250 mg | $143.00 | |||
L-Albizziin, 1 g | sc-218627A | 1 g | $337.00 | |||
L-Albizziin, 5 g | sc-218627B | 5 g | $1617.00 |
