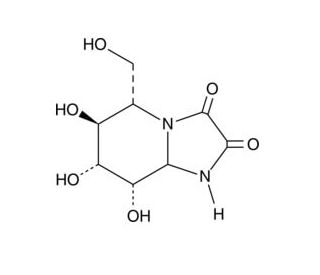
Kifunensine (CAS 109944-15-2)
Produktreferenzen ansehen (25)
Direktverknüpfungen
Kifunensine ist eine chemische Verbindung, die besonders wertvoll im Bereich der Glykobiologie-Forschung ist. Sie wirkt als potenter Inhibitor von Mannosidase I, einem Enzym, das an der Modifikation von Glykoproteinen während ihrer Reifung im endoplasmatischen Retikulum beteiligt ist. Durch die Beeinträchtigung dieses Enzyms wird Kifunensine zur Untersuchung der Faltung und Qualitätskontrolle von Glykoproteinen sowie ihres Transports durch den sekretorischen Weg verwendet. Die Hemmung von Mannosidase I führt zur Produktion von Glykoproteinen mit einem hohen Mannose-Glykan-Profil, was nützlich ist zur Untersuchung von Protein-Faltungsstörungen und zur Verbesserung der Stabilität und Wirksamkeit bestimmter Glykoproteine. Darüber hinaus findet Kifunensine Anwendung in der Entwicklung von Biologika, bei denen die Kontrolle der Glykosylierungsmuster für die Aktivität und Halbwertszeit von Chemikalien entscheidend ist. Es wird auch zur Synthese homogener Glykoproteine für strukturelle und funktionelle Analysen genutzt.
Kifunensine (CAS 109944-15-2) Literaturhinweise
- Eine praktische Synthese von Kifunensin-Analoga als Inhibitoren der Alpha-Mannosidase I des endoplasmatischen Retikulums. | Hering, KW., et al. 2005. J Org Chem. 70: 9892-904. PMID: 16292820
- Glykosidase-Inhibitoren: Inhibitoren der N-verknüpften Oligosaccharidverarbeitung. | Elbein, AD. 1991. FASEB J. 5: 3055-63. PMID: 1743438
- Kifunensin hemmt die Glykoproteinverarbeitung und die Funktion des modifizierten LDL-Rezeptors in Endothelzellen. | Elbein, AD., et al. 1991. Arch Biochem Biophys. 288: 177-84. PMID: 1898016
- Kifunensin, ein starker Inhibitor der Glykoprotein verarbeitenden Mannosidase I. | Elbein, AD., et al. 1990. J Biol Chem. 265: 15599-605. PMID: 2144287
- Synthese von Kifunensin-Thioanaloga und ihre hemmenden Aktivitäten gegen HIV-RT und α-Mannosidase. | Chen, H., et al. 2013. Carbohydr Res. 365: 1-8. PMID: 23159373
- Konformationsanalyse des Mannosidase-Inhibitors Kifunensin: Ein quantenmechanischer und struktureller Ansatz. | Males, A., et al. 2017. Chembiochem. 18: 1496-1501. PMID: 28493500
- Glykoform-Modifikation von sekretierten rekombinanten Glykoproteinen durch Kifunensin-Addition während der transienten Vakuum-Agroinfiltration. | Xiong, Y., et al. 2018. Int J Mol Sci. 19: PMID: 29562594
- In-vivo-Glykan-Engineering durch den Mannosidase-I-Inhibitor (Kifunensin) verbessert die Wirksamkeit von Rituximab, das in Nicotiana benthamiana-Pflanzen hergestellt wird. | Kommineni, V., et al. 2019. Int J Mol Sci. 20: PMID: 30621113
- Die pharmakologische Hemmung des N-gebundenen Glykan-Trimings mit Kifunensin unterbricht den GLUT1-Transport und die Glukoseaufnahme. | Lodge, EK., et al. 2020. Biochimie. 174: 18-29. PMID: 32298759
- Eine Klasse kostengünstiger Alternativen zu Kifunensin zur Erhöhung der N-gebundenen Glykosylierung mit hohem Mannosegehalt für die Produktion monoklonaler Antikörper in Ovarialzellen des chinesischen Hamsters. | Brantley, TJ., et al. 2021. Biotechnol Prog. 37: e3076. PMID: 32888259
- Auswirkungen von Kifunensin auf die Produktion und N-Glykosylierungsmodifikation von Butyrylcholinesterase in einem transgenen Reis-Zellkultur-Bioreaktor. | Macharoen, K., et al. 2020. Int J Mol Sci. 21: PMID: 32962231
- Hemmung des Eindringens von SARS-CoV-2-Viren durch Blockierung der N- und O-Glykanbildung. | Yang, Q., et al. 2020. Elife. 9: PMID: 33103998
- Brefeldin A und Kifunensin modulieren die LPS-induzierte endotheliale Hyperpermeabilität der Lunge in humanen und bovinen Zellen. | Kubra, KT. and Barabutis, N. 2021. Am J Physiol Cell Physiol. 321: C214-C220. PMID: 34161151
- Ein neuer Immunmodulator, FR-900494: Taxonomie, Fermentation, Isolierung sowie physikalisch-chemische und biologische Eigenschaften. | Iwami, M., et al. 1987. J Antibiot (Tokyo). 40: 612-22. PMID: 3610820
- Die Unterbrechung der N-Glykosylierung durch Typ-I-Mannosidase-Inhibitoren verändert die B-Zell-Rezeptor-Signalgebung. | Huang, A., et al. 2022. ACS Pharmacol Transl Sci. 5: 1062-1069. PMID: 36407961
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Kifunensine, 1 mg | sc-201364 | 1 mg | $135.00 | |||
Kifunensine, 5 mg | sc-201364A | 5 mg | $540.00 | |||
Kifunensine, 10 mg | sc-201364B | 10 mg | $1025.00 | |||
Kifunensine, 100 mg | sc-201364C | 100 mg | $6248.00 |
