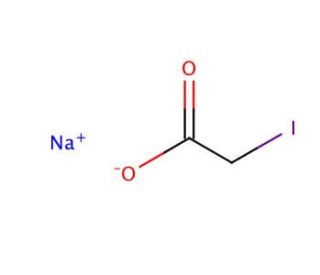
Iodoacetic acid sodium salt (CAS 305-53-3)
Direktverknüpfungen
Das Natriumsalz der Iodoessigsäure, auch bekannt als Natriumiodoacetat, ist eine chemische Verbindung, die in der Biochemie und Laborforschung weit verbreitet ist, aufgrund ihrer Fähigkeit, Cysteinreste in Proteinen zu modifizieren und Cysteinproteasen zu hemmen. Diese Verbindung zeigt eine geringfügige hemmende Wirkung auf spezifische enzymatische Aktivitäten im Hühnerplasma. Sie zeichnet sich durch ihre Löslichkeit in Wasser und Alkohol aus und erscheint als weißer Feststoff. Ihre Rolle erstreckt sich auf verschiedene Forschungsanwendungen, wie Enzymstudien, Analyse der Proteinstruktur und des Stoffwechsels sowie die Erforschung zellulärer Prozesse, einschließlich der Zellsignalgebung und der Funktionalität von Natriumkanälen. Die Fähigkeit des Natriumsalzes der Iodoessigsäure, an Enzymaktive Sites zu binden und ihre katalytischen Funktionen zu behindern, macht es zu einem wertvollen Werkzeug, um Proteine und zelluläre Mechanismen, die DNA- und RNA-Synthese sowie die Genexpression zu verstehen.
Iodoacetic acid sodium salt (CAS 305-53-3) Literaturhinweise
- In vitro-Insulinrückfaltung: Charakterisierung der Zwischenprodukte und des vermuteten Faltungsweges. | Tang, Y., et al. 2007. Sci China C Life Sci. 50: 717-25. PMID: 17914645
- Bevorzugte Nutzung von NADPH als endogener Elektronendonor für die NAD(P)H:Chinon-Oxidoreduktase 1 (NQO1) in intakten pulmonalen arteriellen Endothelzellen. | Bongard, RD., et al. 2009. Free Radic Biol Med. 46: 25-32. PMID: 18848878
- Synthese und Bewertung neuer photoreaktiver Alpha-Aminosäure-Analoga mit sauren und spaltbaren Funktionen. | Bongo, NB., et al. 2009. Bioorg Med Chem Lett. 19: 80-2. PMID: 19026535
- Entwicklung einer Technik zur Plastination von ultradünnen Blättern in Rattenhumerusgelenken mit durch Mononatriumiodoacetat induzierter Osteoarthritis zur Untersuchung der Neovaskularisierung. | Vargas, CA., et al. 2020. Anat Sci Int. 95: 297-303. PMID: 31401788
- Physikalisch-chemische Eigenschaften von Ladungsisomeren rekombinanter menschlicher Superoxiddismutase. | Kajihara, J., et al. 1988. J Biochem. 104: 638-42. PMID: 3241003
- Reduktion und Reoxidation des Neurotoxins II aus dem Skorpion Androctonus australis Hector. | Sabatier, JM., et al. 1987. Int J Pept Protein Res. 30: 125-34. PMID: 3667073
- Interaktion zwischen trypsinähnlichem Enzym aus Streptomyces erythraeus und Hühner-Ovomucoid. | Nagata, K. and Yoshida, N. 1984. J Biochem. 96: 1041-9. PMID: 6394596
- Einfaches Hydrolyseverfahren für alle Aminosäuren, einschließlich Cystein und Tryptophan. | Inglis, AS. 1983. Methods Enzymol. 91: 26-36. PMID: 6855579
- Gleichzeitiger Nachweis von zwei Mechanismen der Immunzerstörung von mit Penicillin behandelten menschlichen roten Blutkörperchen. | Yust, I., et al. 1982. Am J Hematol. 13: 53-62. PMID: 7137166
- Wirkung einiger metallischer Kationen und organischer Verbindungen auf die O-Hexyl-O-2,5-Dichlorphenylphosphoramidat-Hydrolyseaktivität in Hühnerplasma. | Sogorb, MA., et al. 1993. Arch Toxicol. 67: 416-21. PMID: 8215911
- Stoffwechselinhibitoren und Chromosomenverknüpfung | AV Beatty, JW Beatty - American Journal of Botany, 1959 - Wiley Online Library. May 1959. American Journal of Botany. Volume46, Issue5: Pages 317-323.
- Gleichgewichtsfaltung des Schweine-Insulin-Vorläufers in Gegenwart eines Redox-Puffers: Implikationen für die gemeinsamen Zwischenprodukte seiner Entfaltungs/Rückfaltungsprozesse | , et al. 2008,. Protein and Peptide Letters,. Volume 15, Number 9,: pp. 972-979(8).
- Charakterisierung eines intakten Phycoerythrins und seiner gespaltenen funktionellen 14 kDa-Untereinheit aus dem marinen Cyanobakterium Phormidium sp. A27DM | A Parmar, NK Singh, A Kaushal, D Madamwar - Process Biochemistry, 2011 - Elsevier. September 2011,. Process Biochemistry. Volume 46, Issue 9,: Pages 1793-1799.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Iodoacetic acid sodium salt, 25 g | sc-204014 | 25 g | $125.00 |
