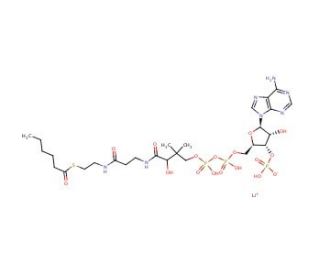
Hexanoyl coenzyme A trilithium salt (CAS 103476-19-3)
Direktverknüpfungen
Hexanoyl-Coenzym-A-Trilithium-Salz ist ein Zwischenprodukt im Prozess des Fettsäurestoffwechsels in der Zelle. Als Coenzym-A-Derivat spielt es eine wichtige Rolle beim Transport und der Aktivierung von Fettsäuren zur Energiegewinnung. Hexanoyl-Coenzym-A-Trilithiumsalz ist an der Übertragung von Acylgruppen während der Beta-Oxidation von Fettsäuren in den Mitochondrien beteiligt. Dieser Prozess führt letztlich zur Erzeugung von ATP, der primären Energiewährung der Zelle. Das Trilithiumsalz des Hexanoyl-Coenzyms A ist an der Biosynthese verschiedener Zellbestandteile wie Phospholipide und Cholesterin beteiligt. Seine Interaktion mit Zellbestandteilen ist sehr spezifisch, da es an Enzyme und Transportproteine bindet, die am Fettsäurestoffwechsel beteiligt sind, und so deren Funktion erleichtert. Hexanoyl-Coenzym-A-Trilithium-Salz ist ein essenzielles Molekül, das die zellulären Prozesse beeinflusst, indem es den Fettsäurestoffwechsel reguliert, der für die Energieerzeugung und die Aufrechterhaltung der zellulären Struktur und Funktion verantwortlich ist.
Hexanoyl coenzyme A trilithium salt (CAS 103476-19-3) Literaturhinweise
- Isolierung und Charakterisierung der drei Polypeptidkomponenten der 4-Chlorbenzoat-Dehalogenase aus Pseudomonas sp. Stamm CBS-3. | Chang, KH., et al. 1992. Biochemistry. 31: 5605-10. PMID: 1610806
- Biosynthese des differenzierungsinduzierenden Faktors von Dictyostelium discoideum durch eine hybride Typ-I-Fettsäure-Typ-III-Polyketid-Synthase. | Austin, MB., et al. 2006. Nat Chem Biol. 2: 494-502. PMID: 16906151
- Die Hexanoyl-CoA-Vorstufe für die Cannabinoid-Biosynthese wird von einem Acyl-aktivierenden Enzym in den Trichomen von Cannabis sativa gebildet. | Stout, JM., et al. 2012. Plant J. 71: 353-65. PMID: 22353623
- Synthese von Fruchtethylestern durch Acyl-Coenzym A: Alkohol-Acyltransferase- und Reverse-Esterase-Aktivitäten in Oenococcus oeni und Lactobacillus plantarum. | Costello, PJ., et al. 2013. J Appl Microbiol. 114: 797-806. PMID: 23216623
- Kristallstrukturen der ersten Kondensationsdomäne der CDA-Synthetase deuten auf Konformationsänderungen während des Synthesezyklus von nichtribosomalen Peptidsynthetasen hin. | Bloudoff, K., et al. 2013. J Mol Biol. 425: 3137-50. PMID: 23756159
- Eine iterative Typ-I-Polyketid-Synthase initiiert die Biosynthese des Antimykoplasma-Mittels Micacocidin. | Kage, H., et al. 2013. Chem Biol. 20: 764-71. PMID: 23790487
- Entdeckung einer allosterischen Inhibitor-Bindungsstelle in 3-Oxo-Acyl-ACP-Reduktase aus Pseudomonas aeruginosa. | Cukier, CD., et al. 2013. ACS Chem Biol. 8: 2518-27. PMID: 24015914
- LC-MS/MS-basierte Analyse von Coenzym A und kurzkettigen Acyl-Coenzym A-Thioestern. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- Fettsäuresynthetase aus der Rinderbrust: Eigenschaften und Produkte. | Kinsella, JE., et al. 1975. Lipids. 10: 227-37. PMID: 27521070
- Fitness auf Stammebene im Darmmikrobiom ist eine sich entwickelnde Eigenschaft von Glykanen und einem einzelnen Metaboliten. | Park, SY., et al. 2022. Cell. 185: 513-529.e21. PMID: 35120663
- Analyse der Gene und des Aromastoffwechsels von Wickerhamomyces anomalus Y-1, isoliert aus einem chinesischen Likörfermentationsstarter. | Shi, X., et al. 2022. Front Microbiol. 13: 891387. PMID: 35586860
- Steigerung der Cannabidiol-Produktion in gentechnisch veränderten Saccharomyces cerevisiae durch Ausnutzung des vakuolären Transporters BPT1. | Qiu, J., et al. 2022. J Agric Food Chem. 70: 12055-12064. PMID: 36122349
- Liposomen-vermittelte enzymatische Synthese von Phosphatidylcholin als Ansatz für selbstreplizierende Liposomen | Peter Kurt Schmidli, Peter Schurtenberger, and Pier Luigi Luisi. 1991. J. Am. Chem. Soc. 113, 21: 8127–8130.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Hexanoyl coenzyme A trilithium salt, 5 mg | sc-215148 | 5 mg | $292.00 | |||
Hexanoyl coenzyme A trilithium salt, 10 mg | sc-215148A | 10 mg | $465.00 |
