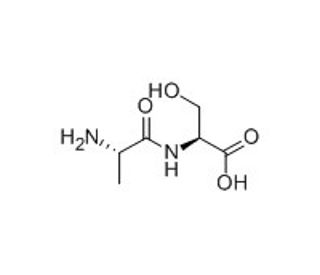
H-Ala-Ser-OH (CAS 3303-41-1)
Direktverknüpfungen
H-Ala-Ser-OH, ein aus Alanin und Serin bestehendes Dipeptid, dient als wertvolle Forschungschemikalie zum Verständnis der Peptidsynthese und der Proteaseaktivität. Dieses einfache Peptid ist von entscheidender Bedeutung für die Untersuchung der Substratspezifität verschiedener Serinproteasen und anderer Enzymklassen, die auf Peptidbindungen einwirken. Forscher nutzen H-Ala-Ser-OH, um die grundlegenden Aspekte der Bildung und des Abbaus von Peptidbindungen zu untersuchen, die für zelluläre Prozesse wie den Proteinumsatz und die Signaltransduktion entscheidend sind. Die Fähigkeit der Verbindung, als Substrat für peptidsynthetisierende Enzyme zu fungieren, ermöglicht auch Einblicke in die Mechanismen der Enzymkatalyse, insbesondere in die Frage, wie die Molekularstruktur die Geschwindigkeit und Spezifität enzymatischer Reaktionen beeinflusst. In biochemischen Studien wird H-Ala-Ser-OH zur Kalibrierung und Optimierung der Bedingungen für die Peptidsynthese und für Assays zur Messung der Enzymaktivität verwendet. Dieses Dipeptid hilft bei der Klärung der Frage, wie sich Veränderungen der Peptidkettenlänge und -zusammensetzung auf die Aktivität von Enzymen auswirken, die für die Aufrechterhaltung der Zellfunktion und -integrität entscheidend sind. H-Ala-Ser-OH trägt zu einem tieferen Verständnis des Peptidverhaltens und der Enzyminteraktion bei und hilft so bei der breiteren Erforschung der biochemischen Wege, an denen Peptide beteiligt sind.
H-Ala-Ser-OH (CAS 3303-41-1) Literaturhinweise
- Affinitäts- und Translokationsbeziehungen von H-X aa-Ser-OH-Dipeptiden über hPEPT1: Bewertung von H-Phe-Ser-OH als Pro-Moiety für Ibuprofen und Benzoesäure-Prodrugs. | Omkvist, DH., et al. 2011. Eur J Pharm Biopharm. 77: 327-31. PMID: 21147219
- Kinetische Studien über die alkalikatalysierte Hydrolyse und Epimerisierung von Modellalkyl- und Hydroxyalkyl-Di- und -Tripeptiden. | Noll, BW., et al. 1974. Biochemistry. 13: 5164-9. PMID: 4433513
- Studien mit Modellsubstanzen zum Mechanismus der Ameisensäure-induzierten reversiblen Inaktivierung von Protein-Enzymen. | Josefsson, L. 1966. Biochim Biophys Acta. 115: 148-59. PMID: 5936231
- Protonen-NMR-, EPR- und Absorptionsspektrenstudien von Palladium(II)- und Kupfer(II)-Komplexen mit L-Alanyl-L-Serin | Kozłowski, H. and Siatecki, Z. 1978. Chemical Physics Letters. 54(3): 498-501.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
H-Ala-Ser-OH, 250 mg | sc-295038 | 250 mg | $218.00 | |||
H-Ala-Ser-OH, 1 g | sc-295038A | 1 g | $667.00 |
