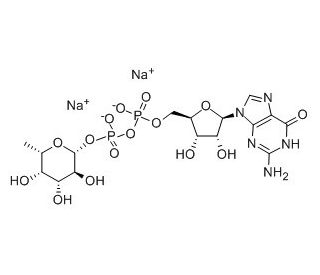
Guanosine 5′-diphospho-β-L-fucose sodium salt (CAS 15839-70-0)
Veja citações de produtos (1)
LINKS RÁPIDOS
O sal sódico de guanosina 5'-difosfo-β-L-fucose é um substrato para a FucT (fucosiltransferase). O sal sódico de guanosina 5′-difosfo-β-L-fucose (GDP-β-L-Fuc) é um carboidrato de ocorrência natural com presença significativa nas paredes celulares de plantas e bactérias. O sal sódico de guanosina 5′-difosfo-β-L-fucose assume um papel fundamental nas vias de biossíntese de glicoproteínas e glicolipídios, garantindo a função celular adequada. Sua indispensabilidade se estende a servir como um intermediário essencial na síntese de polissacarídeos, inclusive aqueles que formam as paredes celulares de bactérias e fungos. Além disso, o sal sódico da guanosina 5′-difosfo-β-L-fucose participa ativamente da biossíntese de polissacarídeos vitais, como a N-acetilglucosamina, a quitina e o sulfato de heparano. O envolvimento do composto também é evidente em sua contribuição para a biossíntese de glicoproteínas e glicolipídios, regulação da adesão celular, modulação das vias de sinalização celular e influência na expressão gênica.
Guanosine 5′-diphospho-β-L-fucose sodium salt (CAS 15839-70-0) Referencias
- Biblioteca de glicopeptídeos marcados com peso molecular: construção eficiente e aplicações. | Ito, H., et al. 2005. Angew Chem Int Ed Engl. 44: 4547-9. PMID: 15981286
- Síntese de análogos de bisubstratos visando a alfa-1,3-fucosiltransferase e suas actividades. | Izumi, M., et al. 2006. Org Biomol Chem. 4: 681-90. PMID: 16467942
- Caracterização bioquímica da α-1,4 fucosiltransferase de Helicobacter pylori: necessidade de iões metálicos, especificidade do substrato dador e estabilidade em solventes orgânicos. | Rabbani, S., et al. 2009. Biometals. 22: 1011-7. PMID: 19565338
- Caracterização de WbiQ: uma α1,2-fucosiltransferase de Escherichia coli O127:K63(B8) e síntese do antigénio do grupo sanguíneo H-type 3. | Pettit, N., et al. 2010. Biochem Biophys Res Commun. 402: 190-5. PMID: 20801103
- Isolamento de bactérias produtoras de fucosiltransferase de ambientes marinhos. | Kajiwara, H., et al. 2012. Microbes Environ. 27: 515-8. PMID: 23100020
- Desenvolvimento de um método de purificação de açúcares de nucleótidos utilizando uma coluna de modo misto e deteção por espetrometria de massa. | Eastwood, H., et al. 2015. J Pharm Biomed Anal. 115: 402-9. PMID: 26279371
- Síntese quimioenzimática de N-glicanos complexos marcados com (13)C como padrões internos para a quantificação absoluta de glicanos por espetrometria de massa. | Echeverria, B., et al. 2015. Anal Chem. 87: 11460-7. PMID: 26482441
- Síntese quimioenzimática divergente de N-Glicanos assimétricos com núcleo fucosilado e com núcleo não modificado. | Li, T., et al. 2016. Chemistry. 22: 18742-18746. PMID: 27798819
- Caracterização bioquímica da α1-3-fucosiltransferase de Helicobacter pylori e sua aplicação na síntese de oligossacáridos fucosilados do leite humano. | Bai, J., et al. 2019. Carbohydr Res. 480: 1-6. PMID: 31132553
- Base estrutural para a especificidade do substrato e a catálise da α1,6-fucosiltransferase. | García-García, A., et al. 2020. Nat Commun. 11: 973. PMID: 32080177
- Uma nova abordagem para identificar isómeros posicionais de glicanos clivados a partir de anticorpos monoclonais. | Dyukova, I., et al. 2021. Analyst. 146: 4789-4795. PMID: 34231555
- Uma GDP-Fuc: β-D-Gal α-1,2-fucosiltransferase essencial e específica do cinetoplasto está localizada na mitocôndria de Trypanosoma brucei. | Bandini, G., et al. 2021. Elife. 10: PMID: 34410224
- A ablação da autofagia mediada por chaperona em pericitos revela novos marcadores de prognóstico do glioblastoma e um tratamento eficaz contra a progressão do tumor. | Molina, ML., et al. 2022. Front Cell Dev Biol. 10: 797945. PMID: 35419364
- Mecanismo da alfa-1,3-fucosiltransferase V humana: a clivagem glicosídica ocorre antes do ataque nucleofílico. | Murray, BW., et al. 1997. Biochemistry. 36: 823-31. PMID: 9020780
Informacoes sobre ordens
| Nome do Produto | Numero de Catalogo | UNID | Preco | Qde | FAVORITOS | |
Guanosine 5′-diphospho-β-L-fucose sodium salt, 1 mg | sc-221696 | 1 mg | $214.00 | |||
Guanosine 5′-diphospho-β-L-fucose sodium salt, 2 mg | sc-221696A | 2 mg | $362.00 |
