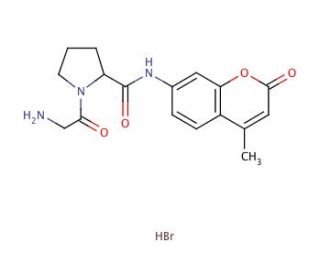
Molekülstruktur von GP-AMC, Fluorogenic Substrate, CAS-Nummer: 115035-46-6
GP-AMC, Fluorogenic Substrate (CAS 115035-46-6)
Alternative Namen:
Gly-Pro-7-amido-4-methylcoumarin hydrobromide; Gly-Pro-AMC
Anwendungen:
GP-AMC, Fluorogenic Substrate wird verwendet, um die Aktivität von CD26, DPP7, DPP8, FAP und PREP zu untersuchen.
CAS Nummer:
115035-46-6
Reinheit:
>97%
Molekulargewicht:
410.3
Summenformel:
C17H19N3O4•HBr
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
GP-AMC ist ein Fluorogen-Substrat mit einer Anregung bei 380 nm und Emission bei 460 nm. Das Substrat wurde verwendet, um die Aktivität von CD26 (DPIV und DPPIV), DPP7 (DPPII/VII), DPRP1 (DPP8), DPRP2 (DPP9), FAP (Fibroblasten-Aktivierungsprotein) und POP/PREP zu untersuchen. Das Substrat wurde in einem Peptid-Assay verwendet, bei dem die Freisetzung von AMC überwacht wurde, sowie in einem in-vitro-Inhibitor-Screening.
GP-AMC, Fluorogenic Substrate (CAS 115035-46-6) Literaturhinweise
- Die vom Haupthistokompatibilitätskomplex der Klasse I präsentierten antigenen Peptide werden in zytosolischen Extrakten hauptsächlich durch Thimet-Oligopeptidase abgebaut. | Saric, T., et al. 2001. J Biol Chem. 276: 36474-81. PMID: 11479311
- Substratspezifität, Hemmung und enzymologische Analyse der rekombinanten menschlichen Glutamatcarboxypeptidase II. | Barinka, C., et al. 2002. J Neurochem. 80: 477-87. PMID: 11905994
- Katalytische Eigenschaften und Hemmung der prolinspezifischen Dipeptidylpeptidasen II, IV und VII. | Leiting, B., et al. 2003. Biochem J. 371: 525-32. PMID: 12529175
- 1-[[(3-Hydroxy-1-adamantyl)amino]acetyl]-2-cyano-(S)-pyrrolidin: ein potenter, selektiver und oral bioverfügbarer Dipeptidylpeptidase IV-Inhibitor mit antihyperglykämischen Eigenschaften. | Villhauer, EB., et al. 2003. J Med Chem. 46: 2774-89. PMID: 12801240
- Charakterisierung der menschlichen Dipeptidylpeptidase IV, exprimiert in Pichia pastoris. Ein struktureller und mechanistischer Vergleich zwischen dem rekombinanten menschlichen und dem gereinigten Schweineenzym. | Bär, J., et al. 2003. Biol Chem. 384: 1553-63. PMID: 14719797
- Diastereoselektive Synthese und konfigurationsabhängige Aktivität von (3-substituierten Cycloalkyl)glycinpyrrolididen und -thiazolididen als Dipeptidylpeptidase IV-Inhibitoren. | Ashton, WT., et al. 2004. Bioorg Med Chem Lett. 14: 859-63. PMID: 15012982
- Bindungskinetik und Dauer der In-vivo-Wirkung neuer Prolyl-Oligopeptidase-Hemmer. | Venäläinen, JI., et al. 2006. Biochem Pharmacol. 71: 683-92. PMID: 16405869
- Antidiabetische, antiglykotische und antioxidative Aktivitäten von ethanolischem Samenextrakt aus Passiflora edulis und Piceatannol in vitro. | Dos Santos, FAR., et al. 2022. Molecules. 27: PMID: 35807309
- In-vivo- und In-vitro-Vergleich des DPP-IV-hemmenden Potenzials von Nahrungsproteinen unterschiedlicher Herkunft nach gastrointestinaler Verdauung. | Fleury, L., et al. 2022. Int J Mol Sci. 23: PMID: 35955493
Substrat von:
CD26, DPP7, DPRP1, DPRP2, Enzyme, FAP, Fluorogenic, Peptide, POP, und PREP.Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
GP-AMC, Fluorogenic Substrate, 5 mg | sc-201157 | 5 mg | $133.00 |
