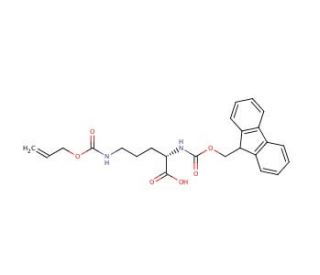
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7)
Direktverknüpfungen
Fmoc-Orn(Alloc)-OH stellt ein Derivat des Aminosäure-Derivats Ornithin dar, das natürlich vorkommt und als Zwischenstufe im Stickstoffstoffwechsel im Harnstoffzyklus eine Rolle spielt. Es wird weit verbreitet in der organischen Synthese und Biochemie eingesetzt und ist sehr vielseitig. Es dient mehreren Zwecken, einschließlich der Protein- und Peptidsynthese sowie als Ausgangsstoff für die Synthese verschiedener Verbindungen. In der wissenschaftlichen Forschung findet Fmoc-Orn(Alloc)-OH umfangreiche Anwendungen, insbesondere in der Peptid- und Proteinsynthese. Seine Nützlichkeit liegt in der Einführung verschiedener funktioneller Gruppen in Peptide und Proteine. Darüber hinaus wird diese Verbindung zur Synthese anderer Verbindungen wie kleiner Moleküle und Polymere verwendet. Seine Fähigkeit, eine breite Palette funktioneller Gruppen in diese Verbindungen einzuführen, ist sehr vorteilhaft. Das Wirkungsmechanismus von Fmoc-Orn(Alloc)-OH basiert auf seiner Reaktivität mit Aminosäuren und anderen Molekülen. Durch seine Interaktion mit einer Aminosäure bildet es eine kovalente Bindung, die als Peptidbindung bekannt ist und das Verknüpfen von Aminosäuren zur Bildung von Peptiden und Proteinen ermöglicht. Darüber hinaus kann Fmoc-Orn(Alloc)-OH durch seine Reaktionen mit kleinen Molekülen und Polymeren kovalente Bindungen mit ihnen eingehen.
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7) Literaturhinweise
- Synthese und spezifische Antikörperbildung für Glykopeptide mit Arginin-N-GlcNAcylierung. | Pan, M., et al. 2014. Angew Chem Int Ed Engl. 53: 14517-21. PMID: 25353391
- Spezifischer tandemmassenspektrometrischer Nachweis von AGE-modifizierten Argininresten in Peptiden. | Schmidt, R., et al. 2015. J Mass Spectrom. 50: 613-24. PMID: 25800199
- Selektives Aufspüren von Pyrophosphat in physiologischen Medien unter Verwendung von Zink(II)dipicolylamino-funktionalisierten Peptiden. | Zwicker, VE., et al. 2015. Org Biomol Chem. 13: 7822-9. PMID: 26107804
- Synthetische Peptide, die die Bindungsstelle der menschlichen Acetylcholinesterase für ihren Inhibitor Fasciculin 2 nachahmen. | Kafurke, U., et al. 2015. J Pept Sci. 21: 723-30. PMID: 26200472
- Die Auflösung der α-glykosidischen Bindung des Arginin-rhamnosylierten Translationsdehnungsfaktors P löst die Bildung des ersten ArgRha-spezifischen Antikörpers aus. | Li, X., et al. 2016. Chem Sci. 7: 6995-7001. PMID: 28451135
- Erkennung von Dimethylarginin-Analoga durch das Tandem-Tudor-Domänen-Protein Spindlin1. | Porzberg, MRB., et al. 2022. Molecules. 27: PMID: 35164245
- Biokompatible und selektive Erzeugung von bizyklischen Peptiden. | Ullrich, S., et al. 2022. Angew Chem Int Ed Engl. 61: e202208400. PMID: 35852030
- Pegylierte Peptide. II. Festphasensynthese von pegylierten Amino-, Carboxy- und Seitenkettenpeptiden. | Lu, YA. and Felix, AM. 1994. Int J Pept Protein Res. 43: 127-38. PMID: 8200730
- Eine Doppelrolle der Phenylboronsäure als Rezeptor für Kohlenhydrate und als Quencher für das benachbarte Pyren-Fluorophor | Lok Nath Neupane, Chuda Raj Lohani, Jeongho Kim, Keun-Hyeung Lee. 2013. Tetrahedron. 69: 11057-11063.
- Totalsynthese der TRADD-Todesdomäne mit Arginin-N-GlcNAcylierung durch native chemische Bindung auf Hydrazidbasis | Ye Wu a b 1, Yulei Li c 1, Wei Cong a, Yan Zou b, Xiang Li b, Honggang Hu a. 2020. Chinese Chemical Letters. 31: 107-110.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Fmoc-Orn(Alloc)-OH, 5 g | sc-235198 | 5 g | $156.00 |
