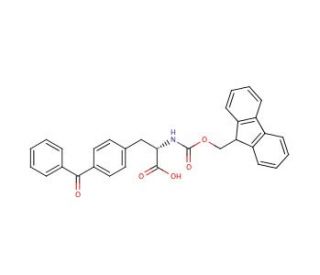
Fmoc-Bpa-OH (CAS 117666-96-3)
Direktverknüpfungen
Fmoc-Bpa-OH ist eine Verbindung, die als vielseitiger Baustein in der Peptidsynthese fungiert. Sie fungiert als Schutzgruppe für die Aminogruppe von Aminosäuren und ermöglicht eine selektive Entschützung und anschließende Kopplungsreaktionen. Der Wirkmechanismus von Fmoc-Bpa-OH umfasst die Bildung stabiler Amidbindungen mit Aminosäuren, was den schrittweisen Aufbau von Peptiden mit hoher Reinheit und Ausbeute ermöglicht. Fmoc-Bpa-OH erleichtert die Synthese komplexer Peptide, indem es ein Mittel zur Kontrolle der Reaktivität spezifischer funktioneller Gruppen bietet, was zu einem präzisen Aufbau von Peptidketten führt. Seine Rolle bei der Peptidsynthese umfasst den Schutz von Aminogruppen, die Verhinderung unerwünschter Nebenreaktionen und die Gewährleistung der erfolgreichen Bildung von Peptidbindungen. Der Wirkmechanismus von Fmoc-Bpa-OH auf molekularer Ebene ermöglicht die effiziente und kontrollierte Synthese von Peptiden mit maßgeschneiderten Sequenzen und Strukturen und macht es zu einem nützlichen Werkzeug in der Forschung und Entwicklung der Peptidchemie.
Fmoc-Bpa-OH (CAS 117666-96-3) Literaturhinweise
- Doppelte Rolle der proapoptotischen BAD bei der Insulinsekretion und dem Überleben der Betazellen. | Danial, NN., et al. 2008. Nat Med. 14: 144-53. PMID: 18223655
- Synthese und spektroskopische Charakterisierung von Peptidliganden mit Photoaffinität zur Untersuchung der Interaktion zwischen Rhodopsin und Protein. | Chen, Y., et al. 2008. Photochem Photobiol. 84: 831-8. PMID: 18282180
- Die Hysterese des Gatings unterstreicht die Sensibilisierung von TRPV3-Kanälen. | Liu, B., et al. 2011. J Gen Physiol. 138: 509-20. PMID: 22006988
- Manipulation der Aktivierung des Y-Rezeptor-Subtyps von kurzen Neuropeptid-Y-Analoga durch Einführung von Carbaboranen. | Hofmann, S., et al. 2013. Neuropeptides. 47: 59-66. PMID: 23352609
- Direkte Aktivierung der proapoptotischen BAK in voller Länge. | Leshchiner, ES., et al. 2013. Proc Natl Acad Sci U S A. 110: E986-95. PMID: 23404709
- Chemische Synthese von kohlenwasserstoffgestapelten Peptiden für die Erforschung von Proteininteraktionen und die gezielte therapeutische Anwendung. | Bird, GH., et al. 2011. Curr Protoc Chem Biol. 3: 99-117. PMID: 23801563
- Die Bindung des PA1b-Inhibitors an die Untereinheiten c und e der vakuolären ATPase offenbart seinen insektiziden Mechanismus. | Muench, SP., et al. 2014. J Biol Chem. 289: 16399-408. PMID: 24795045
- Photo-Lysin fängt Proteine ein, die posttranslationale Lysinmodifikationen binden. | Yang, T., et al. 2016. Nat Chem Biol. 12: 70-2. PMID: 26689789
- Middle-Down- und chemische Proteomik-Ansätze zur Aufdeckung der Dynamik von Histon-H4-Modifikationen im Zellzyklus: Markierungsfreie Semi-Quantifizierung von Histon-Schwanzpeptidmodifikationen einschließlich Phosphorylierung und hochempfindliche Erfassung von Histon-PTM-bindenden Proteinen unter Verwendung photoreaktiver Crosslinker. | Yamamoto, K., et al. 2015. Mass Spectrom (Tokyo). 4: A0039. PMID: 26819910
- Kurze HIV-1-Integrase-Peptide, die von einer viralen Protein-R-Sequenz abgeleitet sind. | Zhao, XZ., et al. 2018. Molecules. 23: PMID: 30049955
- Zellfreie Expression und Photo-Vernetzung des menschlichen Neuropeptid-Y2-Rezeptors. | Kögler, LM., et al. 2019. Front Pharmacol. 10: 176. PMID: 30881304
- Selektive bakterielle Ausrichtung und infektionsbedingte Freisetzung von antibiotischen Colistin-Konjugaten. | Tegge, W., et al. 2021. Angew Chem Int Ed Engl. 60: 17989-17997. PMID: 34097810
- Konformationsdynamik in Verbindung mit Domänenschließung und Substratbindung erklärt den Mechanismus der allosterischen Regulierung von ERAP1. | Maben, Z., et al. 2021. Nat Commun. 12: 5302. PMID: 34489420
- Identifizierung der Interaktionsstelle zwischen Semaphorin-3A und seinem hemmenden Peptid. | Kretschmer, K., et al. 2023. J Pept Sci. 29: e3460. PMID: 36285908
- Die prophylaktische und therapeutische Impfung schützt die Gesundheit der Spermien vor durch Chlamydia muridarum verursachten Anomalien. | Bryan, ER., et al. 2023. Biol Reprod. 108: 758-777. PMID: 36799886
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Fmoc-Bpa-OH, 1 g | sc-223992 | 1 g | $309.00 |
