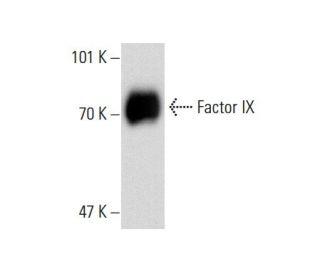

Factor IX Antikörper (GMA-138): sc-65952
- Factor IX Antikörper GMA-138 ist ein monoklonales IgG1 aus der Maus, verwendet in 1 wissenschaftlichen Veröffentlichungen, in einer Menge von 100 µg/ml
- gezogen gegen Factor IX aus der Spezies human
- Empfohlen für die Detektion von Factor IX aus der Spezies human per WB und IP
- Aktuell testen wir noch unsere Sekundärantikörper um das beste Bindeprotein für diesen Primärantikörper Factor IX (GMA-138) zu finden. Kontaktieren Sie uns bitte, wenn Sie Fragen hierzu haben sollten.
Direktverknüpfungen
Siehe auch...
Nach einer Gewebeverletzung beinhaltet die Hämostase die Freisetzung essentieller plasmatischer Prokoagulantien (Prothrombin, Faktoren X, IX, V und VIII), die an einer Blutgerinnungskaskade beteiligt sind, die zur Bildung unlöslicher Fibrinblutgerinnsel und zur Förderung der Thrombozytenaggregation führt. Der Gerinnungsfaktor IX (plasmatische Thromboplastinkomponente, F9, F.IX, HEMB) ist ein vitamin K-abhängiger, einzelsträngiger Serinprotease, der in der Leber synthetisiert und als inaktiver Vorstufe im Blutkreislauf zirkuliert. Durch die proteolytische Spaltung von Faktor IX durch Faktor XIa wird Faktor IXa generiert, ein aktiver Serinprotease, der aus einer 145 Aminosäure-Leichte Kette und einer 236 Aminosäure-katalytischen Schwerkette durch Disulfidbindungen verbunden ist. Genetische Veränderungen am Faktor IX-Locus, wie Punktmutationen, Insertionen und Deletionen, können zu Hämophilie B, auch als Weihnachtskrankheit bekannt, führen.
Alexa Fluor® ist ein Markenzeichen von Molecular Probes Inc., OR., USA
LI-COR® und Odyssey® sind Markenzeichen von LI-COR Biosciences
Factor IX Antikörper (GMA-138) Literaturhinweise:
- Faktor IX-Mutanten mit erhöhter katalytischer Aktivität. | Hartmann, R., et al. 2009. J Thromb Haemost. 7: 1656-62. PMID: 19656280
- Populationspharmakokinetische Modellierung der Faktor IX-Aktivität nach Verabreichung von rekombinantem Faktor IX bei Patienten mit Hämophilie B. | Suzuki, A., et al. 2016. Haemophilia. 22: e359-66. PMID: 27353956
- Eine einzige synonyme Mutation in Faktor IX verändert die Proteineigenschaften und liegt der Hämophilie B zugrunde. | Simhadri, VL., et al. 2017. J Med Genet. 54: 338-345. PMID: 28007939
- Die EGF-Domäne des Gerinnungsfaktors IX begünstigt die Freisetzung von Phosphatidylserin. | Hidai, C., et al. 2017. Cell Biol Int. 41: 374-383. PMID: 28150893
- Entwicklung eines Inhibitors bei einem älteren Patienten mit schwerem Faktor-IX-Mangel, der mit ALPROLIX, einem rekombinanten Faktor-IX-Fc-Fusionsprotein, behandelt wurde. | Comerford, C., et al. 2021. Haemophilia. 27: e484-e486. PMID: 33215798
- Proteolytische Inaktivierung des Blutgerinnungsfaktors IX durch Thrombin. | Kisiel, W., et al. 1985. Blood. 66: 1302-8. PMID: 4063523
- Postnatale Entwicklung von Faktor IX. | Schettini, F., et al. 1980. Acta Paediatr Scand. 69: 53-8. PMID: 7368912
- Humaner Faktor IX korrigiert die Blutungsdiathese von Mäusen mit Hämophilie B. | Kung, SH., et al. 1998. Blood. 91: 784-90. PMID: 9446637
- Einige menschliche Inhibitor-Antikörper stören die Bindung von Faktor VIII an Faktor IX. | Zhong, D., et al. 1998. Blood. 92: 136-42. PMID: 9639509
- Die neutrophile Elastase spaltet den menschlichen Faktor IX und erzeugt ein aktiviertes Faktor IX-ähnliches Produkt ohne gerinnungsfördernde Funktion. | Samis, JA., et al. 1998. Blood. 92: 1287-96. PMID: 9694717
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Factor IX Antikörper (GMA-138) | sc-65952 | 100 µg/ml | $322.00 |

