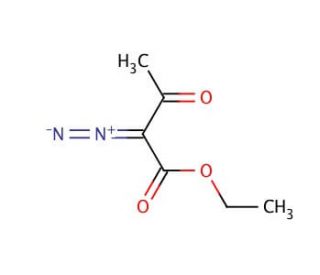
Ethyl diazoacetoacetate (CAS 2009-97-4)
Direktverknüpfungen
Ethyldiazoacetoacetat ist eine organische Verbindung mit vielseitigen Anwendungen in Wissenschaft und Industrie. Es handelt sich um einen Ester, der aus der Kombination von Butansäure und 2-Diazo-3-oxobutan entsteht. Darüber hinaus wurde es ausgiebig als vielversprechendes Reagenz in der organischen Synthese untersucht, und Forscher haben sein Potenzial als Katalysator in bestimmten chemischen Reaktionen erforscht. Darüber hinaus wurden seine Eigenschaften als Fluoreszenzfarbstoff für mögliche Anwendungen in verschiedenen bildgebenden Verfahren untersucht. Es wird vermutet, dass die Verbindung bei bestimmten chemischen Reaktionen als Protonendonator fungiert und das Ergebnis der Reaktion beeinflusst. Darüber hinaus steigert das nachgewiesene Lewis-Säure-Verhalten der Verbindung in ausgewählten organischen Reaktionen ihr Potenzial als wirksamer Katalysator weiter.
Ethyl diazoacetoacetate (CAS 2009-97-4) Literaturhinweise
- Ein neuer Weg zu gehinderten tertiären Aminen. | Yang, M., et al. 2001. J Org Chem. 66: 6729-33. PMID: 11578227
- Stereoselektive Synthese von hochfunktionalisierten alpha-Diazo-beta-ketoalkanoaten über katalytische Eintopf-Mukaiyama-Aldol-Reaktionen. | Zhou, L. and Doyle, MP. 2010. Org Lett. 12: 796-9. PMID: 20102172
- Rh(III)-katalysierte Synthese von multisubstituierten Isochinolin- und Pyridin-N-Oxiden aus Oximen und Diazoverbindungen | Shi, Z., et al. 2013. J Am Chem Soc. 135: 12204-7. PMID: 23889167
- Rh(III)-katalysierte Synthese von 1-Aminoindolderivaten aus 2-Acetyl-1-arylhydrazinen und Diazoverbindungen in Wasser. | Liang, Y., et al. 2014. Chem Commun (Camb). 50: 6130-3. PMID: 24777073
- Ursprüngliche Reaktivität von α-Diazo-β-Ketoestern, katalysiert durch CpRu-Komplexe. | Tortoreto, C., et al. 2014. Chimia (Aarau). 68: 243-7. PMID: 24983607
- Azirinium-Ylide von α-Diazoketonen und 2H-Azirinen auf dem Weg zu 2H-1,4-Oxazinen: Dreiringöffnung vs. 1,5-Cyclisierung. | Rostovskii, NV., et al. 2015. Beilstein J Org Chem. 11: 302-12. PMID: 25815084
- Regioselektive Synthesen von 1,2-Benzothiazinen durch rhodiumkatalysierte Annulationsreaktionen. | Cheng, Y. and Bolm, C. 2015. Angew Chem Int Ed Engl. 54: 12349-52. PMID: 25873036
- Regioselektive Synthese von multisubstituierten Isochinolonen und Pyridonen über Rh(III)-katalysierte Annulationsreaktionen | Shi, L., et al. 2015. Chem Commun (Camb). 51: 17277-80. PMID: 26463232
- Mechanistische Einblicke in die Rh(III)-katalysierte C-H-Aktivierung von 2-Acetyl-1-Arythydrazinen in Wasser. | Wu, W., et al. 2017. J Phys Chem A. 121: 1825-1832. PMID: 28182407
- Synthese von [5,6]-bicyclischen Heterocyclen mit einem Stickstoffatom mit Ringverbindung: Rhodium(III)-katalysierte C-H-Funktionalisierung von Alkenyl-Azolen. | Halskov, KS., et al. 2017. Angew Chem Int Ed Engl. 56: 9183-9187. PMID: 28586164
- Synthese von 2,3-Benzodiazepinen über Rh(III)-katalysierte C-H-Funktionalisierung von N-Boc-Hydrazonen mit Diazoketoestern. | Wang, J., et al. 2017. Org Lett. 19: 3640-3643. PMID: 28641013
- Cp*Ir(iii)-katalysierte C-H/N-H-Funktionalisierung von Sulfoximinen für die Synthese von 1,2-Benzothiazinen bei Raumtemperatur. | Aher, YN., et al. 2018. Chem Commun (Camb). 54: 6288-6291. PMID: 29850690
- Approfondimento teorico del meccanismo, della regioselettività e dell'effetto del gruppo sostituente nella sintesi catalizzata da Rh di 1,2-benzotiazine da NH-sulfossimine e composti diazoici. | Yan, J., et al. 2018. Org Biomol Chem. 16: 5321-5331. PMID: 29999079
- Cp*Ir(III)-Katalysierte C-H/O-H-Funktionalisierung von Salicylaldehyden für die Synthese von Chromonen bei Raumtemperatur. | Lade, DM., et al. 2019. J Org Chem. 84: 9188-9195. PMID: 31273978
- Direkte Beobachtung von Ylid- und Enol-Zwischenprodukten, die in Konkurrenz zur Wolff-Umlagerung von photoangeregtem Ethyldiazoacetoacetat gebildet werden. | Phelps, R. and Orr-Ewing, AJ. 2020. J Am Chem Soc. 142: 7836-7844. PMID: 32267699
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Ethyl diazoacetoacetate, 1 g | sc-228064 | 1 g | $270.00 |
