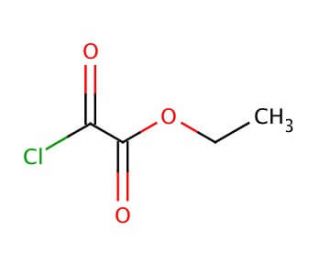
Ethyl chlorooxoacetate (CAS 4755-77-5)
Direktverknüpfungen
Ethylchlorooxoacetat ist eine chemische Verbindung, die in der organischen Synthese als Acylierungsreagenz dient. Es wirkt als Elektrophil und reagiert mit Nukleophilen wie Aminen, Alkoholen und Thiolen, um Ester, Amide bzw. Thioester zu bilden. Die Wirkungsweise besteht in der Übertragung der Acylgruppe auf das Nucleophil, was zur Bildung des gewünschten acylierten Produkts führt. Ethylchlorooxoacetat ist für seine Fähigkeit bekannt, ein breites Spektrum an Nukleophilen effizient zu acylieren, was es vielseitig für die Synthese verschiedener organischer Verbindungen einsetzbar macht. Seine Reaktivität und Selektivität bei Acylierungsreaktionen machen es zu einem wichtigen Hilfsmittel bei der Entwicklung neuer Moleküle und Materialien. In der Entwicklung spielt es eine Rolle bei der Veränderung funktioneller Gruppen und der Schaffung verschiedener chemischer Strukturen.
Ethyl chlorooxoacetate (CAS 4755-77-5) Literaturhinweise
- Synthese und biologische Bewertung von Chromoncarboxamiden als Calpain-Inhibitoren. | Lee, KS., et al. 2005. Bioorg Med Chem Lett. 15: 2857-60. PMID: 15911268
- Synthese und Bewertung von 3-Anilino-Quinoxalinonen als Glykogenphosphorylase-Inhibitoren. | Dudash, J., et al. 2005. Bioorg Med Chem Lett. 15: 4790-3. PMID: 16143521
- Generierung von Oxamsäure-Bibliotheken: Malariamittel und Inhibitoren der Laktatdehydrogenase von Plasmodium falciparum. | Choi, SR., et al. 2007. J Comb Chem. 9: 292-300. PMID: 17316052
- Eine effiziente und skalierbare Synthese von substituierten Phenanthrenchinonen durch intramolekulare Friedel-Crafts-Reaktion von Imidazoliden. | Yoshikawa, N., et al. 2007. Org Lett. 9: 4103-6. PMID: 17880225
- Inhibitoren der HIV-1-Anheftung. Teil 2: Ein erster Überblick über Indol-Substitutionsmuster. | Meanwell, NA., et al. 2009. Bioorg Med Chem Lett. 19: 1977-81. PMID: 19251416
- Synthese, biologische Bewertung und Docking-Analyse einer neuen Familie von 1-Methyl-1H-Pyrrol-2,5-Dionen als hochwirksame und selektive Cyclooxygenase-2 (COX-2)-Inhibitoren. | Kim, KJ., et al. 2014. Bioorg Med Chem Lett. 24: 1958-62. PMID: 24656662
- 2,2,2-Trifluorethylchlorooxoacetat - Universelles Reagenz für die parallele Eintopfsynthese von N(1)-Aryl-N(2)-Alkyl-substituierten Oxamiden. | Bogolubsky, AV., et al. 2015. ACS Comb Sci. 17: 615-22. PMID: 26325360
- Optische Kontrolle von AMPA-Rezeptoren mit Hilfe eines photoschaltbaren Chinoxalin-2,3-dion-Antagonisten. | Barber, DM., et al. 2017. Chem Sci. 8: 611-615. PMID: 28451208
- Einführung einer funktionellen α-Ketoestergruppe durch Pt-katalysierte direkte C-H-Acylierung mit Ethylchlorooxoacetat. | Javed, E., et al. 2020. ACS Omega. 5: 8393-8402. PMID: 32309750
- Rhodium(I)-NHC-Komplexe mit zweizähnigen bis-heteroatomaren Acidato-Liganden als gem-selektive Katalysatoren für die Alkin-Dimerisierung. | Galiana-Cameo, M., et al. 2020. Chemistry. 26: 9598-9608. PMID: 32374897
- Bor(III)-Subchlorine vom A2B- und A3-Typ, abgeleitet von meso-Diethoxycarbonyltripyrran: Synthese und photophysikalische Erforschung. | Soman, R., et al. 2021. J Org Chem. 86: 10280-10287. PMID: 34264670
- Effizienter Zugang zu aliphatischen Estern durch photokatalysierte Alkoxycarbonylierung von Alkenen mit Alkyloxalylchloriden. | Chen, JQ., et al. 2021. Nat Commun. 12: 5328. PMID: 34493725
- Synthese von Ester-substituierten Indolo[2,1-a]isochinolinen über photokatalysierte Alkoxycarbonylierungs-/Cyclisierungsreaktionen. | Chen, JQ., et al. 2022. Org Lett. 24: 642-647. PMID: 34985296
- Design und Synthese neuartiger spirozyklischer Carbonsäuren als potente und oral bioverfügbare DGAT1-Inhibitoren und ihre biologische Bewertung. | Koul, S., et al. 2022. Bioorg Med Chem Lett. 62: 128632. PMID: 35189320
- Durch sichtbares Licht induzierte 1,7-Enn-Dicyclisierung: Synthese von Ester-substituierten Benzo[j]phenanthridinen. | Chen, JQ., et al. 2023. Org Lett. 25: 1978-1983. PMID: 36912498
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Ethyl chlorooxoacetate, 25 g | sc-239923 | 25 g | $36.00 | |||
Ethyl chlorooxoacetate, 100 g | sc-239923A | 100 g | $87.00 |
