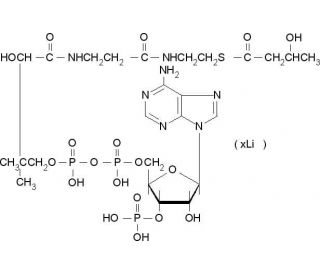
DL-β-Hydroxybutyryl coenzyme A lithium salt (CAS 103404-51-9)
Produktreferenzen ansehen (1)
Direktverknüpfungen
Das Lithiumsalz von DL-β-Hydroxybutyryl-Coenzym A dient als zentraler Ausgangsstoff für die Synthese von bakteriellen Polyhydroxyalkanoaten (PHB) durch die Wirkung von Polyhydroxybutyrat (PHB)-Synthasen. Diese Verbindung spielt eine Rolle im breiteren Kontext der mikrobiellen Biosynthese und der Produktion biologisch abbaubarer Polymere, was ihre Bedeutung für die biotechnologische Forschung zur Entwicklung nachhaltiger Materialien unterstreicht. Ihre Beteiligung am Fettsäurestoffwechsel und an der Energiegewinnung unterstreicht ihre grundlegende Bedeutung in biochemischen Abläufen, die für zelluläre Prozesse zentral sind. DL-β-Hydroxybutyryl-Coenzym-A-Lithiumsalz ist nicht nur für die Synthese von PHB, einem Biopolymer, das aufgrund seiner biologisch abbaubaren Eigenschaften von Interesse ist, von entscheidender Bedeutung, sondern stellt auch einen Schlüsselknotenpunkt in den Stoffwechselnetzwerken dar, die die Umwandlung von Lipidsubstraten in wertvolle biotechnologische Produkte ermöglichen, und bietet somit Einblicke in die Optimierung von Strategien des Metabolic Engineering zur Verbesserung der Biosyntheseeffizienz.
DL-β-Hydroxybutyryl coenzyme A lithium salt (CAS 103404-51-9) Literaturhinweise
- Nachweis der Polyhydroxyalkanoat-Synthase-Aktivität auf einem Polyacrylamid-Gel. | Sheu, DS., et al. 2009. Anal Biochem. 393: 62-6. PMID: 19527674
- Nachweis von kovalenten und nicht-kovalenten Zwischenprodukten in der Polymerisationsreaktion, die von einer C149S Klasse III Polyhydroxybutyrat-Synthase katalysiert wird. | Li, P., et al. 2009. Biochemistry. 48: 9202-11. PMID: 19711985
- Charakterisierung der hochaktiven Polyhydroxyalkanoat-Synthase von Chromobacterium sp. Stamm USM2. | Bhubalan, K., et al. 2011. Appl Environ Microbiol. 77: 2926-33. PMID: 21398494
- LC-MS/MS-basierte Analyse von Coenzym A und kurzkettigen Acyl-Coenzym A-Thioestern. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- Entschlüsselung und Entwicklung der Produktion von 23,24-Bisnorcholensäure-Steroiden im Sterinstoffwechsel. | Xu, LQ., et al. 2016. Sci Rep. 6: 21928. PMID: 26898409
- Herstellung von Polyhydroxyalkanoaten (PHA) aus synthetischen Abfällen mit Pseudomonas pseudoflava: Analyse der PHA-Synthase-Enzymaktivität von P. pseudoflava und P. palleronii. | Venkateswar Reddy, M., et al. 2017. Bioresour Technol. 234: 99-105. PMID: 28319778
- Optimierung der Überexpression eines Chaperonproteins der Steroid-C25-Dehydrogenase zur biochemischen und biophysikalischen Charakterisierung. | Niedzialkowska, E., et al. 2017. Protein Expr Purif. 134: 47-62. PMID: 28343996
- Hydrophile Interaktionsflüssigkeitschromatographie-Tandem-Massenspektrometrie-Analyse von Malonyl-Coenzym A in Brustkrebszellkulturen unter Verwendung einer Online-Festphasenextraktion. | Schriewer, A., et al. 2017. J Sep Sci. 40: 4303-4310. PMID: 28877409
- Funktionelle Charakterisierung eines neuen Gens, Hc-dhs-28, und seine Rolle beim Schutz des Wirts nach einer Infektion mit Haemonchus contortus durch Regulierung der Diapausenbildung. | Yang, Y., et al. 2020. Int J Parasitol. 50: 945-957. PMID: 32858035
- Histondeacetylase 3 koppelt Mitochondrien, um die IL-1β-abhängige Entzündung durch Konfiguration der Fettsäureoxidation anzutreiben. | Chi, Z., et al. 2020. Mol Cell. 80: 43-58.e7. PMID: 32937100
- Auswirkungen der Ketogenese auf den Leberstoffwechsel durch Proteomik der Lysin-β-Hydroxybutyrylierung. | Koronowski, KB., et al. 2021. Cell Rep. 36: 109487. PMID: 34348140
- Die quantitative subzelluläre Acyl-CoA-Analyse zeigt einen unterschiedlichen Kernstoffwechsel und eine isoleucinabhängige Histonpropionylierung. | Trefely, S., et al. 2022. Mol Cell. 82: 447-462.e6. PMID: 34856123
- β-Hydroxybutyrat reduziert die Wiederaufnahme der kokainbedingten Ortspräferenz durch CaMKII-α β-Hydroxybutyrylierung im Hippocampus. | Li, H., et al. 2022. Cell Rep. 41: 111724. PMID: 36450263
- Eine quantitative zytochemische Methode zur Messung der Beta-Hydroxyacyl-CoA-Dehydrogenase-Aktivität im Herzmuskel der Ratte. | Chambers, DJ., et al. 1982. Histochemistry. 75: 67-76. PMID: 7118583
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
DL-β-Hydroxybutyryl coenzyme A lithium salt, 10 mg | sc-214926 | 10 mg | $410.00 | |||
DL-β-Hydroxybutyryl coenzyme A lithium salt, 25 mg | sc-214926A | 25 mg | $890.00 | |||
DL-β-Hydroxybutyryl coenzyme A lithium salt, 50 mg | sc-214926B | 50 mg | $1795.00 |
