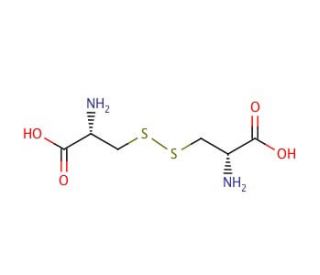
D-Cystine (CAS 349-46-2)
Direktverknüpfungen
D-Cystin wird vor allem wegen seiner Anwendungen in der Biochemie und Molekularbiologie erforscht, wobei der Schwerpunkt auf seiner Rolle in der Proteinstruktur und -funktion liegt. Bei dieser Verbindung handelt es sich um eine dimere Aminosäure, die durch die Oxidation von zwei Cysteinmolekülen gebildet wird, wodurch eine Disulfidbindung entsteht, die für die Stabilität vieler Proteine verantwortlich ist. In Studien mit D-Cystin wird häufig sein Verhalten bei Redoxreaktionen und seine Fähigkeit zur Bildung und Aufrechterhaltung von Disulfidbrücken in Proteinen untersucht, die für die ordnungsgemäße Faltung und Funktion von Proteinen unerlässlich sind. Darüber hinaus ist die Beteiligung von D-Cystin an zellulären Prozessen wie der Signalübertragung und -regulierung ein wichtiges Untersuchungsgebiet. Die Forschung untersucht auch, wie sich Modifikationen von D-Cystin auf biologische Systeme auswirken, was zum Verständnis der zellulären Reaktionen auf oxidativen Stress und andere Umweltfaktoren beiträgt.
D-Cystine (CAS 349-46-2) Literaturhinweise
- Biochemische Selektionssysteme für Säugetierzellen: die essentiellen Aminosäuren. | Naylor, SL., et al. 1976. Somatic Cell Genet. 2: 93-111. PMID: 1028167
- Peptidi ciclici a doppia elica: progettazione, sintesi e struttura cristallina di conformeri a otto figure speculari di un peptide ciclico contenente cistina, legato all'adamantano (Adm-Cyst)(3). | Ranganathan, D., et al. 2000. J Org Chem. 65: 4415-22. PMID: 10891146
- Thermostabile S-Alkylcystein-alpha, beta-Lyase aus einem Thermophilen: Reinigung und Eigenschaften. | Kamitani, H., et al. 1990. Agric Biol Chem. 54: 2069-76. PMID: 1368609
- L-CYSTIN-BEDARF FÜR DIE PRODUKTION DES COXSACKIE B3-VIRUS IN KULTIVIERTEN AFFENHERZZELLEN. | TYNDALL, RL. and LUDWIG, EH. 1963. J Bacteriol. 85: 1339-45. PMID: 14047227
- L-Cystin hemmt Aspartat-beta-Semialdehyd-Dehydrogenase durch kovalente Bindung an das essenzielle 135Cys des Enzyms. | Alvarez, E., et al. 2004. Biochim Biophys Acta. 1696: 23-9. PMID: 14726201
- Vergleichende Artenverwertung und Toxizität von schwefelhaltigen Aminosäuren. | Baker, DH. 2006. J Nutr. 136: 1670S-1675S. PMID: 16702338
- Unterschiedliche Wirkungen von endogenen Cysteinanaloga auf die periphere thermische Nozizeption bei intakten Ratten. | Pathirathna, S., et al. 2006. Pain. 125: 53-64. PMID: 16782275
- Dimere und monomere Tenside, die von schwefelhaltigen Aminosäuren abgeleitet sind. | Faustino, CM., et al. 2010. J Colloid Interface Sci. 351: 472-7. PMID: 20800236
- Reinigung und Charakterisierung von Cystin-Lyase a aus Broccoli-Blütenständen. | Ukai, K. and Sekiya, J. 1997. Biosci Biotechnol Biochem. 61: 1890-5. PMID: 27396740
- Die Rolle schwefelhaltiger Aminosäuren bei der Superoxidproduktion und der Veränderung von Lipoprotein niedriger Dichte durch glatte Arterienmuskelzellen. | Heinecke, JW., et al. 1987. J Biol Chem. 262: 10098-103. PMID: 3038867
- Reinigung und Charakterisierung von Clostridium sticklandii D-Selenocystin-alpha, beta-Lyase. | Esaki, N., et al. 1988. J Bacteriol. 170: 751-6. PMID: 3338973
- Penicillin-unempfindlicher Einbau von D-Aminosäuren in Zellwandpeptidoglycan beeinflusst die Menge des gebundenen Lipoproteins in Escherichia coli. | Tsuruoka, T., et al. 1984. J Bacteriol. 160: 889-94. PMID: 6389516
- Verwendung und Sicherheit von isomeren schwefelhaltigen Aminosäuren bei Mäusen. | Friedman, M. and Gumbmann, MR. 1984. J Nutr. 114: 2301-10. PMID: 6502274
- Aminosäuren und Derivate der Thiazol-4-Carbonsäure als Bestandteile von Thiopeptin B. | Muramatsu, I., et al. 1977. J Antibiot (Tokyo). 30: 383-7. PMID: 885796
- Inaktivierung von Phosphoenolypyruvat-Carboxykinase (GTP) durch Leberextrakte. | Ballard, FJ. and Hopgood, MF. 1976. Biochem J. 154: 717-24. PMID: 942393
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
D-Cystine, 5 g | sc-255056 | 5 g | $90.00 |
