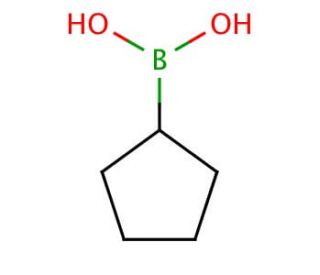
Molekülstruktur von Cyclopentylboronic acid, CAS-Nummer: 63076-51-7
Cyclopentylboronic acid (CAS 63076-51-7)
CAS Nummer:
63076-51-7
Molekulargewicht:
113.95
Summenformel:
C5H11BO2
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
Cyclopentylboronsäure ist eine Boronsäure, die als Organokatalysator in der Synthese aromatischer Verbindungen verwendet wird. Sie zeigt Reaktivität gegenüber Chlor und kann in Kreuzkupplungsreaktionen mit anderen Boronsäuren, Halogeniden und Trifluoriden eingreifen. Bemerkenswerterweise ermöglicht diese vielseitige Verbindung die Synthese funktioneller aromatischer Kohlenwasserstoffe durch palladium- oder nickelkatalysierte Reaktionen, die Tosylate oder Mesylate als Ausgangsstoffe verwenden. Der Einsatz von Cyclopentylboronsäure als Organokatalysator hat sich als effizienter im Kupplungsprozess erwiesen.
Cyclopentylboronic acid (CAS 63076-51-7) Literaturhinweise
- Kreuzkupplungsreaktionen von chiralen sekundären Organoboronsäureestern unter Beibehaltung der Konfiguration. | Imao, D., et al. 2009. J Am Chem Soc. 131: 5024-5. PMID: 19301820
- Unkomplizierter synthetischer Zugang zu gem-diaurierten und digoldierten σ,π-Acetylid-Spezies. | Gómez-Suárez, A., et al. 2013. Angew Chem Int Ed Engl. 52: 938-42. PMID: 23180680
- Enantioselektive 1,4-Addition von Cyclopropylboronsäure, katalysiert durch Rhodium/chirale Dien-Komplexe. | Takechi, R. and Nishimura, T. 2015. Chem Commun (Camb). 51: 8528-31. PMID: 25892197
- 1,n-Bisborylalkane über radikalische Bor-Migration. | Wang, D., et al. 2020. J Am Chem Soc. 142: 9119-9123. PMID: 32363871
- Die Passerini-Reaktion von Boronsäuren ermöglicht die Synthese von α-Hydroxyketonen. | Yang, K., et al. 2021. Nat Commun. 12: 441. PMID: 33469014
- Ein Borabgabe-Antikörper (BDA) mit borspezifischen Rückständen: Neue Perspektiven für die Borneutroneneinfangtherapie durch eine In-Silico-Untersuchung. | Rondina, A., et al. 2021. Cells. 10: PMID: 34831449
- Cp*Rh(III)-katalysierte C-H Arylierung von Ferrocenethionamiden mit Arylboronsäuren für die Synthese von Aryl-Ferrocenen. | Wang, Y., et al. 2023. Chem Asian J. 18: e202201180. PMID: 36495085
- Ruphos-vermittelte Suzuki-Kreuzkupplung von sekundären Alkyltrifluoroboraten | Adri van den Hoogenband a, Jos H.M. Lange a, Jan Willem Terpstra a, Melle Koch b, Gerben M. Visser b, Martin Visser a, Ties J. Korstanje a, Johann T.B.H. Jastrzebski c. 2008. Tetrahedron Letters. 49: 4122-4124.
- Kupfer(I)-3-Methylsalicylat vermittelt die Chan-Lam-N-Arylierung von Heterocyclen | Abdelbasset A. Farahat & David W. Boykin. 2015. Synthetic Communications. 45: 245-252.
- Synthese von asymmetrischen Dibenzothiophensulfonatestern | John T. Petroff II, Ryan D. McCulla. 2016. Tetrahedron Letters. 57: 4723-4726.
- Phthalimid-getragener Schwefeltransfer zur Synthese von unsymmetrischen Disulfanen durch Kupferkatalyse | Jiaoxia Zou, Jinhong Chen, Tao Shi*, Yongsheng Hou, Fei Cao, Yongqiang Wang, Xiaodong Wang, Zhong Jia, Quanyi ZhaoQuanyi ZhaoSchool of Pharmacy, Lanzhou University, West Donggang Road, No. 199, Lanzhou 730000, China, et al. 2019. ACS Catal. 9: 11426–11430.
- Durch sichtbares Licht induzierte chemoselektive Reaktionen von Chinoxalin-2(1H)-onen mit Alkylboronsäuren unter Luft/N2-Atmosphäre | Lingling Yao a, Defeng Zhu a, Lei Wang a b, Jie Liu a, Yicheng Zhang a, Pinhua Li a c. 2021. Chinese Chemical Letters. 32: 4033-4037.
- Übergangsmetall-freie DMAP-vermittelte aromatische Veresterung von Amiden mit Organoboronsäuren | Tao Wang, Yanqing Wang, Kai Xu, Yuheng Zhang, Jiarui Guo, Prof. Lantao Liu. 2021. European Journal of Organic Chemistry. 14: 3274-3277.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Cyclopentylboronic acid, 1 g | sc-234480 | 1 g | $48.00 |
