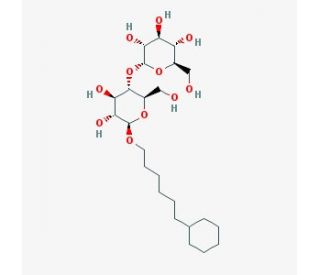
Cyclohexyl-n-hexyl-β-D-maltoside (CAS 228579-27-9)
Direktverknüpfungen
Cyclohexyl-n-hexyl-β-D-maltosid, ein nichtionisches Detergens, hat sich aufgrund seiner einzigartigen Eigenschaften und vielfältigen Anwendungsmöglichkeiten zu einem wichtigen Werkzeug in der Membranproteinforschung entwickelt. Als mildes Detergens löst es Membranproteine effektiv auf, wobei ihre native Struktur und Funktion erhalten bleiben, was es ideal für die Reinigung von Membranproteinen und Kristallisationsstudien macht. Seine Fähigkeit, die Umgebung der Lipiddoppelschicht zu imitieren, erleichtert die Extraktion und Stabilisierung von Membranproteinen und ermöglicht deren biochemische und biophysikalische Charakterisierung. Darüber hinaus wurde Cyclohexyl-n-hexyl-β-D-maltosid ausgiebig in verschiedenen strukturbiologischen Techniken eingesetzt, darunter Röntgenkristallographie, Kernspinresonanzspektroskopie (NMR) und Kryo-Elektronenmikroskopie (Kryo-EM), um die dreidimensionalen Strukturen von Membranproteinen aufzuklären. Durch die Bereitstellung einer wohldefinierten membranähnlichen Umgebung erhöht dieses Detergens die Stabilität von Membranproteinen und verbessert die Auflösung von Strukturstudien, wodurch unser Verständnis ihrer molekularen Mechanismen und Wechselwirkungen verbessert wird. Darüber hinaus hat Cyclohexyl-n-hexyl-β-D-maltosid Anwendungen in der Arzneimittelforschung und -entwicklung gefunden, insbesondere in Screening-Assays und beim strukturbasierten Wirkstoffdesign für Membranproteine, was seine Bedeutung für die biomedizinische Forschung und pharmazeutische Innovation unterstreicht.
Cyclohexyl-n-hexyl-β-D-maltoside (CAS 228579-27-9) Literaturhinweise
- Prokaryote Multidrug-Efflux-Proteine der Major Facilitator Superfamilie: verstärkte Expression, Reinigung und Charakterisierung. | Ward, A., et al. 2001. J Mol Microbiol Biotechnol. 3: 193-200. PMID: 11321573
- Hemmung der SHV-1-Beta-Lactamase durch Sulfone: kristallografische Beobachtung von zwei Reaktionsintermediaten mit Tazobactam. | Kuzin, AP., et al. 2001. Biochemistry. 40: 1861-6. PMID: 11327849
- Reinigung, Kristallisierung und vorläufige Beugungsstudien von AcrB, einem Multidrug-Efflux-Protein der Innenmembran. | Pos, KM. and Diederichs, K. 2002. Acta Crystallogr D Biol Crystallogr. 58: 1865-7. PMID: 12351840
- Auswirkung von Membranstörungen auf die Aktivität und Phasenverteilung der Inositol-Phosphorylceramid-Synthase; Entwicklung eines neuen Assays. | Aeed, PA., et al. 2004. Biochemistry. 43: 8483-93. PMID: 15222759
- Mikrobielle Arzneimittel-Effluxproteine der Major-Facilitator-Superfamilie. | Saidijam, M., et al. 2006. Curr Drug Targets. 7: 793-811. PMID: 16842212
- Oligomeres Verhalten der RND-Transporter CusA und AcrB in mizellarer Lösung von Detergenzien. | Stroebel, D., et al. 2007. Biochim Biophys Acta. 1768: 1567-73. PMID: 17467658
- Expression, Reinigung und Aktivitäten der gesamten Familie der intakten Membransensorkinasen aus Enterococcus faecalis. | Ma, P., et al. 2008. Mol Membr Biol. 25: 449-73. PMID: 18785057
- Das Kind ist mit dem Bade ausgeschüttet: Die AcrB-Kontamination ist ein großes Problem bei der Kristallisation von Membranproteinen. | Veesler, D., et al. 2008. Acta Crystallogr Sect F Struct Biol Cryst Commun. 64: 880-5. PMID: 18931428
- Produktion und biophysikalische Charakterisierung des CorA-Transporters aus Methanosarcina mazei. | Veesler, D., et al. 2009. Anal Biochem. 388: 115-21. PMID: 19233118
- Entscheidende Rolle von Asp408 im Protonen-Translokationsweg des Multidrug-Transporters AcrB: Nachweis durch ortsgerichtete Mutagenese und Carbodiimid-Markierung. | Seeger, MA., et al. 2009. Biochemistry. 48: 5801-12. PMID: 19425588
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Cyclohexyl-n-hexyl-β-D-maltoside, 1 g | sc-280651 | 1 g | $439.00 |
