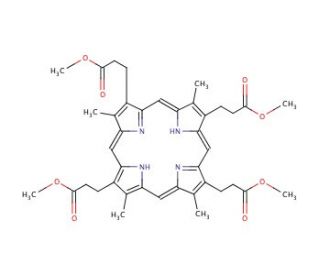
Coproporphyrin III tetramethyl ester (CAS 5522-63-4)
Direktverknüpfungen
Coproporphyrin-III-Tetramethylester ist ein chemisch synthetisiertes Porphyrinderivat, das durch die Methylierung der Carboxylgruppen an den Propionsäure-Seitenketten von Coproporphyrin III gekennzeichnet ist, wodurch veresterte Formen entstehen. Durch diese Modifikation wird seine Lipophilie erhöht, was seine Einbindung in verschiedene experimentelle Systeme erleichtert. Als Bestandteil der großen Porphyrinfamilie spielt es eine zentrale Rolle bei der Untersuchung photodynamischer Prozesse und der Nachahmung biologischer Systeme, insbesondere im Zusammenhang mit der Photosynthese und den Mechanismen der Elektronentransferkette. Die Tetramethylester-Modifikation ermöglicht es den Forschern, die Struktur-Funktions-Beziehungen innerhalb der Porphyrin-Komplexe zu untersuchen, was zur Aufklärung der Rolle beiträgt, die diese Verbindungen in natürlichen und künstlichen Lichtsammelsystemen spielen. Seine einzigartigen Eigenschaften machen es zu einem unverzichtbaren Werkzeug bei der Synthese von Materialien auf Porphyrinbasis für Anwendungen in der Photovoltaik, der Sensorik und der Entwicklung neuartiger photoempfindlicher Verbindungen, die als Schlüsselsubstanz für die Erforschung lichtvermittelter chemischer Reaktionen und Energieumwandlungsprozesse dienen.
Coproporphyrin III tetramethyl ester (CAS 5522-63-4) Literaturhinweise
- Spektrale Absorption und Fluoreszenz der Coproporphyrin-Isomere I und III und die Schmelzpunkte ihrer Methylester. | Jope, EM. and O'brien, JR. 1945. Biochem J. 39: 239-44. PMID: 16747894
- Spektrale Absorptionskoeffizienten einiger Porphyrine im Soret-Band-Bereich. | Rimington, C. 1960. Biochem J. 75: 620-3. PMID: 16748818
- Identifizierung von Tetrapyrrolverbindungen, die von Rhodobacter sphaeroides ausgeschieden werden, und von Quellen für die Methylwasserstoffe des von R. sphaeroides biosynthetisierten Bakteriochlorophylls a, basierend auf der 13C-NMR-Spektralanalyse von Coproporphyrin III-Tetramethylester. | Iida, K., et al. 2007. Chem Pharm Bull (Tokyo). 55: 1067-9. PMID: 17603203
- Die Auswirkung von Variationen in der Struktur des Porphyrin-Photosensibilisators auf die Photohämolyse. | de Paolis, A., et al. 1985. Biochem J. 226: 757-66. PMID: 2985045
- Pyrrole und verwandte Verbindungen. XXXII. Biosynthese von Protoporphyrin-IX aus Coproporphyrinogen-3. | Cavaleiro, JA., et al. 1974. J Chem Soc Perkin 1. 10: 1188-94. PMID: 4212292
- In vitro-Nahrungsbedarf von Nippostrongylus brasiliensis. II. Auswirkungen von Hämverbindungen, Porphyrinen und Gallenpigmenten auf die freilebenden Stadien. | Bolla, RI., et al. 1974. Comp Biochem Physiol B. 48: 147-57. PMID: 4598741
- Porphyrin-Überproduktion durch Pseudomonas denitrificans: Wesentlichkeit von Betain und Stimulation durch Ethionin. | Demain, AL. and White, RF. 1971. J Bacteriol. 107: 456-60. PMID: 5113597
- Zinkphyrin, ein neues Coproporphyrin III mit Zink aus Streptomyces sp. | Toriya, M., et al. 1993. J Antibiot (Tokyo). 46: 196-200. PMID: 8436554
- Ein primitiver Weg der Porphyrin-Biosynthese und Enzymologie in Desulfovibrio vulgaris. | Ishida, T., et al. 1998. Proc Natl Acad Sci U S A. 95: 4853-8. PMID: 9560192
- Mercurierungsreaktionen von Porphyrinen: neue effiziente Synthesen von Harderoporphyrin und Isoharderoporphyrin | Kevin M. Smith and Kevin C. Langry. 1980. J. Chem. Soc., Chem. Commun. 5: 217-218.
- Dealkylierung bei der elektronenstoßmassenspektrometrischen Analyse von N- monoalkylierten Porphyrinmethylestern | and Andrew G. Smith, Peter B. Farmer. 1982. Biological Mass Spectrometry. 9, 3: 111-114.
- Elektrophile Mercurierungsreaktionen von Derivaten von Deuteroporphyrin IX: neue Synthesen von Coproporphyrin III, Harderoporphyrin, Isoharderoporphyrin und S-411 Porphyrin (Dehydrocoproporphyrin) | Kevin M. Smith and Kevin C. Langry. 1983. J. Org. Chem. 48, 4: 500–506.
- Zeitaufgelöste Lumineszenz-Pulsradiolyse-Bestimmung der Anteile von Porphyrin-Photosensibilisatoren-Tripletts, die beim Quenchen durch Triplett-Sauerstoff im Grundzustand zu angeregtem Singulett-Sauerstoff führen | EJ Land. 1991. Journal of Photochemistry and Photobiology A: Chemistry. 61, 2: 165-170.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Coproporphyrin III tetramethyl ester, 1 mg | sc-214758 | 1 mg | $105.00 | |||
Coproporphyrin III tetramethyl ester, 5 mg | sc-214758A | 5 mg | $355.00 |
