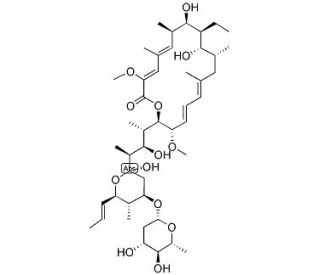
Concanamycin C (CAS 81552-34-3)
Produktreferenzen ansehen (4)
Direktverknüpfungen
Concanamycin C mit der CAS-Nummer 81552-34-3 ist eine chemische Verbindung, die zur Klasse der Concanamycine gehört, einer Gruppe von Makrolid-Antibiotika, die von dem Bakterium Streptomyces neyagawaensis stammen. Ähnlich wie andere Mitglieder seiner Familie wirkt Concanamycin C in erster Linie als Hemmstoff der vakuolären H+-ATPase (V-ATPase). Die V-ATPase ist ein Enzymkomplex, der für die Ansäuerung verschiedener intrazellulärer Kompartimente wie Lysosomen, Endosomen und dem Golgi-Apparat entscheidend ist. Die Hemmung der V-ATPase durch Concanamycin C führt zu einer Unterbrechung des Ansäuerungsprozesses, der für zahlreiche zelluläre Funktionen wie die Proteinsortierung, die Reifung von Enzymvorläufern und den Abbau zellulärer Abfälle unerlässlich ist. In der Forschung wurde Concanamycin C eingesetzt, um die physiologischen und biochemischen Folgen veränderter intrazellulärer pH-Werte zu untersuchen. Durch die Blockierung der Funktion von V-ATPasen können Forscher die Auswirkungen auf zelluläre Prozesse wie Autophagie, Endozytose und die zelluläre Reaktion auf Umweltstress untersuchen. Diese Verbindung trägt zur Aufklärung der komplizierten Mechanismen bei, durch die Zellen ihren internen pH-Wert aufrechterhalten und den Umsatz verschiedener Biomoleküle steuern, und wirft so ein Licht auf die grundlegenden Aspekte der Zellbiologie und der Organellenfunktion.
Concanamycin C (CAS 81552-34-3) Literaturhinweise
- Zelluläre Rolle der V-ATPase in Neurospora crassa: Analyse von Mutanten, die gegen Concanamycin resistent sind oder denen die katalytische Untereinheit A fehlt. | Bowman, EJ. and Bowman, BJ. 2000. J Exp Biol. 203: 97-106. PMID: 10600678
- Die Störung von vma-1, dem Gen, das für die katalytische Untereinheit der vakuolären H(+)-ATPase kodiert, verursacht schwere morphologische Veränderungen in Neurospora crassa. | Bowman, EJ., et al. 2000. J Biol Chem. 275: 167-76. PMID: 10617601
- Semisynthetische Derivate von Concanamycin A und C als Inhibitoren von ATPasen des V- und P-Typs: Struktur-Aktivitäts-Untersuchungen und Entwicklungen von Photoaffinitätssonden. | Dröse, S., et al. 2001. Biochemistry. 40: 2816-25. PMID: 11258892
- Ein Modell für den Proteolipidring und die Bafilomycin/Concanamycin-Bindungsstelle in der vakuolären ATPase von Neurospora crassa. | Bowman, BJ., et al. 2006. J Biol Chem. 281: 31885-93. PMID: 16912037
- Die aktive Ausscheidung über das Verdauungsgewebe geht auf die Entstehung der Ausscheidungsorgane zurück. | Andrikou, C., et al. 2019. PLoS Biol. 17: e3000408. PMID: 31356592
- Struktur-Aktivitäts-Beziehungen von natürlichen und halbsynthetischen Plecomacroliden deuten auf unterschiedliche Wege für die HIV-1-Immunumgehung und die vakuoläre ATPase-abhängige lysosomale Ansäuerung hin. | McCauley, M., et al. 2024. J Med Chem. 67: 4483-4495. PMID: 38452116
- Isolierung und Charakterisierung der Concanamycine A, B und C. | Kinashi, H., et al. 1984. J Antibiot (Tokyo). 37: 1333-43. PMID: 6511660
- Die basolaterale Sekretion des Amyloid-Vorläuferproteins in Madin-Darby-Hundenieren wird durch Veränderungen des intrazellulären pH-Wertes und durch die Einführung einer mit der familiären Alzheimer-Krankheit assoziierten Mutation gestört. | De Strooper, B., et al. 1995. J Biol Chem. 270: 4058-65. PMID: 7876155
- Hemmende Wirkung von modifizierten Bafilomycinen und Concanamycinen auf Adenosinetriphosphatasen vom P- und V-Typ. | Dröse, S., et al. 1993. Biochemistry. 32: 3902-6. PMID: 8385991
- Stoffwechselprodukte von Mikroorganismen. Teil 265. Prelactone C und B, Oligoketide aus Streptomyces, die Concanamycine und Bafilomycine produzieren. | Bindseil, et al. 1993. Helvetica chimica acta. 76.1: 150-157.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Concanamycin C, 100 µg | sc-203006 | 100 µg | $280.00 | |||
Concanamycin C, 500 µg | sc-203006A | 500 µg | $785.00 |
