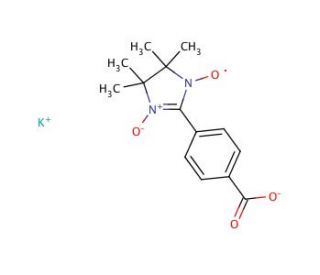
Molekülstruktur von Carboxy-PTIO, potassium salt, CAS-Nummer: 148819-94-7
Carboxy-PTIO, potassium salt (CAS 148819-94-7)
Produktreferenzen ansehen (10)
Alternative Namen:
Carboxy-PTIO, potassium salt also known as 2-(4-Carboxyphenyl)-4,4,5,5-tetramethylimidazoline-1-oxyl-3-oxide potassium salt
Anwendungen:
Carboxy-PTIO, potassium salt ist ein wasserlöslicher und stabiler Stickoxid-Radikalfänger, der mit Stickoxid reagiert
CAS Nummer:
148819-94-7
Reinheit:
≥98%
Molekulargewicht:
315.39
Summenformel:
C14H16N2O4•K
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Publikationen
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
Carboxy-PTIO, Kaliumsalz, reagiert mit Stickstoffmonoxid, um Carboxy-PTI-Derivate zu bilden, die wiederum die NOS (Stickstoffmonoxidsynthase) hemmen. Carboxy-PTIO, Kaliumsalz, ist ein Kaliumsalz, das sich als stabile Imidazolinoxyl-N-Oxidradikalverbindung erwiesen hat. Studien haben gezeigt, dass Carboxy-PTIO, Kaliumsalz, ein Stickstoffmonoxid-Antagonist ist und infolgedessen konzentrationsabhängig Relaxation von Mäuseaorten verursacht. Weitere Studien legen nahe, dass Carboxy-PTIO, Kaliumsalz, bei Konzentrationen von 300 μM oder mehr tatsächlich die Relaxation, die durch nitrergische Nervenstimulation ausgelöst wird, leicht verstärkt.
Carboxy-PTIO, potassium salt (CAS 148819-94-7) Literaturhinweise
- Entspannung der glatten Gefäßmuskulatur durch Stickstoffoxid-Donatoren: ein Vergleich mit Acetylcholin, Stickstoffoxid und Nitroxyl-Ionen. | Wanstall, JC., et al. 2001. Br J Pharmacol. 134: 463-72. PMID: 11588100
- Die Rolle von Stickstoffmonoxid in Gehirnregionen, die mit Abwehrreaktionen in Verbindung stehen. | Guimarães, FS., et al. 2005. Neurosci Biobehav Rev. 29: 1313-22. PMID: 16095696
- Molekulare Mechanismen und therapeutische Strategien der chronischen Nierenschädigung: physiologische Rolle des Angiotensin-II-induzierten oxidativen Stresses im Nierenmedulla. | Mori, T., et al. 2006. J Pharmacol Sci. 100: 2-8. PMID: 16404134
- Hemmung der Biofilmbildung von Staphylokokken durch Nitrit. | Schlag, S., et al. 2007. J Bacteriol. 189: 7911-9. PMID: 17720780
- Die Produktion von Stickstoffmonoxid und seine funktionelle Verbindung mit OIPK in der durch Chitooligosaccharid ausgelösten Abwehrreaktion des Tabaks. | Zhang, H., et al. 2011. Plant Cell Rep. 30: 1153-62. PMID: 21336582
- Markierungsfreie quantitative Proteomik-Analyse der Reaktion von Baumwollblättern auf Stickstoffmonoxid. | Meng, Y., et al. 2011. J Proteome Res. 10: 5416-32. PMID: 22029526
- S-Sulfhydratisierung/Desulfhydratisierung und S-Nitrosylierung/Denitrosylierung: ein gemeinsames Paradigma für die Gasotransmitter-Signalgebung durch H2S und NO. | Lu, C., et al. 2013. Methods. 62: 177-81. PMID: 23811297
- Lipopolysaccharid-induzierte Kreuztoleranz gegen Nieren-Ischämie-Reperfusionsschäden wird durch die über den Hypoxie-induzierbaren Faktor-2α regulierte Stickstoffoxidproduktion vermittelt. | He, K., et al. 2014. Kidney Int. 85: 276-88. PMID: 24025643
- Schnelles NOS-1-Stickoxid und die Bildung von Peroxynitrit wirken als Signalgeber für die induzierbare NOS-2-Expression in glatten Gefäßmuskelzellen. | Scheschowitsch, K., et al. 2015. Pharmacol Res. 100: 73-84. PMID: 26253183
- Die cholinerge und nitrerge Neurotransmission im dorsalen Hippocampus moduliert die kardiale Baroreflexfunktion bei Ratten. | Ferreira-Junior, NC., et al. 2020. Eur J Neurosci. 51: 991-1010. PMID: 31626713
- Ein neuer Stickstoffmonoxid-Fänger, ein Imidazolinoxyl-N-Oxid-Derivat, und seine Auswirkungen in der Pathophysiologie und Mikrobiologie. | Maeda, H., et al. 1995. Curr Top Microbiol Immunol. 196: 37-50. PMID: 7543398
- Vasodilatatorische Wirkung von Carboxy-2-phenyl-4,4,5,5-tetramethylimidazolin-1-oxyl im Koronarkreislauf: in vivo und in vitro Studien. | Tsunoda, R., et al. 1994. Eur J Pharmacol. 262: 55-63. PMID: 7813579
- Antagonistische Wirkung von Imidazolinoxyl-N-Oxiden gegen den vom Endothel abgeleiteten Relaxing Factor/.NO durch eine Radikalreaktion. | Akaike, T., et al. 1993. Biochemistry. 32: 827-32. PMID: 8422387
- Unterscheidung zwischen NO und dem nitrergen Transmitter, aber nicht zwischen NO und EDRF, durch das NO-Fangmittel Carboxy-PTIO. | Rand, MJ. and Li, CG. 1995. Br J Pharmacol. 116: 1906-10. PMID: 8528578
- Superoxidanionen, Radikalfänger und nitrerge Neurotransmission. | Gibson, A. and Lilley, E. 1997. Gen Pharmacol. 28: 489-93. PMID: 9147013
Inhibitor von:
Enzyme, und NOS.Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Carboxy-PTIO, potassium salt, 10 mg | sc-202985 | 10 mg | $97.00 | |||
Carboxy-PTIO, potassium salt, 50 mg | sc-202985A | 50 mg | $305.00 | |||
Carboxy-PTIO, potassium salt, 250 mg | sc-202985B | 250 mg | $969.00 |
