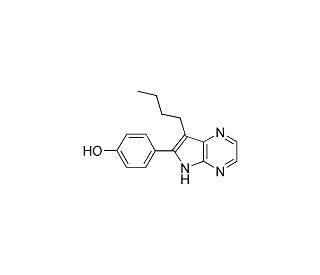
Aloisine A 의 분자 구조, CAS 번호: 496864-16-5
Aloisine A (CAS 496864-16-5)
대체 이름:
RP107; 7-n-Butyl-6-(4-hydroxyphenyl)[5H]pyrrolo[2,3-b]pyrazine
적용:
Aloisine A CDK1, CDK2, CDK5, GSK-3 알파 및 JNK의 억제제입니다.
CAS 등록번호:
496864-16-5
순도:
≥95%
분자량:
267.33
분자식:
C16H17N3O
연구용으로만 사용가능합니다. 진단이나 치료용으로 사용불가합니다.
* 참조분석증명서대량의 측정 데이터(함수량포함).
빠른 링크
주문정보
설명
기술정보
안전정보
SDS 및 분석 증명서
알로이신 A는 CDK(cyclin-dependent kinase)와 GSK-3(glycogen synthase kinase-3)의 매우 강력하고 선택적인 억제제이다. 그것의 억제 작용은 세포 주기의 G1 단계와 G2 단계 모두에서 세포를 체포함으로써 효과적으로 세포 증식을 억제한다. 특정 세포 주기 체크포인트를 차단함으로써 G1 단계와 G2 단계 모두에서 세포 증식을 크게 방해한다. 더욱이, 그것의 GSK-3β 및 JNK 억제 능력은 중요한 신호 전달 경로에 대한 그것의 영향을 더욱 확장시킨다.
Aloisine A (CAS 496864-16-5) 참고자료
- 새로운 CDK/GSK-3 억제제 계열인 알로이신. SAR 연구, CDK2와 결합한 결정 구조, 효소 선택성 및 세포 효과. | Mettey, Y., et al. 2003. J Med Chem. 46: 222-36. PMID: 12519061
- 암의 세포 분열 주기를 표적으로 합니다: CDK 및 세포 주기 체크포인트 키나아제 억제제. | Collins, I. and Garrett, MD. 2005. Curr Opin Pharmacol. 5: 366-73. PMID: 15964238
- 항증식 활성을 가진 유망한 단백질 키나아제 억제제인 새로운 5,7-치환 6-아미노-5H-피롤로[3,2-b]피라진-2,3-디카르보니트릴을 개발했습니다. | Dubinina, GG., et al. 2006. Eur J Med Chem. 41: 727-37. PMID: 16675067
- 야생형, G551D 및 F508del 낭포성 섬유증 막 통과 전도도 조절제 염화물 채널의 서브마이크로몰 친화성 활성화제로서 피롤로[2,3-b]피라진 유도체 발견. | Noel, S., et al. 2006. J Pharmacol Exp Ther. 319: 349-59. PMID: 16829626
- 친화성 크로마토그래피에 의한 알로이신 A의 잠재적 세포 표적 확인. | Corbel, C., et al. 2009. Bioorg Med Chem. 17: 5572-82. PMID: 19596197
- 숙주 세포 단백질을 표적으로 하는 화합물은 배양, 생체 외, SCID-Hu 마우스에서 수두 대상포진 바이러스 복제를 방지합니다. | Rowe, J., et al. 2010. Antiviral Res. 86: 276-85. PMID: 20307580
- 시험관 내에서 사이클린 의존성 키나아제의 저분자 억제제의 항혈관 신생 잠재력. | Zahler, S., et al. 2010. Angiogenesis. 13: 239-49. PMID: 20706783
- 세포 사멸 미만 농도에서 LNCaP 인간 전립선암 세포에서 인데루빈 유도체의 증식 및 안드로겐 효과. | Rivest, P., et al. 2011. Chem Biol Interact. 189: 177-85. PMID: 21111724
- 비독성 변형 피롤로[2,3-b]피라진 유도체에 의한 야생형, F508del- 및 G551D-CFTR 염화물 채널의 자극. | Dannhoffer, L., et al. 2011. Front Pharmacol. 2: 48. PMID: 21897819
- 키나아제 제어는 높은 수준의 유도된 NF-κB 활성에도 불구하고 HIV-1의 재활성화를 방지합니다. | Wolschendorf, F., et al. 2012. J Virol. 86: 4548-58. PMID: 22345467
- 체세포의 증식 속도는 리프로그래밍 효율에 영향을 미칩니다. | Xu, Y., et al. 2013. J Biol Chem. 288: 9767-9778. PMID: 23439651
- CDK5/p25 복합체에 대한 억제제의 결합 메커니즘: 자유 에너지 계산 및 순위 집계 분석. | Wu, Q., et al. 2013. Mol Inform. 32: 251-60. PMID: 27481520
- PXR 의존적 CYP450 대사 및 유도를 위한 CDK 억제를 통한 간세포주 Huh7의 빠른 성숙. | Bulutoglu, B., et al. 2019. Sci Rep. 9: 15848. PMID: 31676845
의 억제제:
Cdk2, Cdk5, GSK-3 alpha, JNK, Ser/Thr Protein Kinase.의 활성화자:
CFTR.주문정보
| 제품명 | 카탈로그 번호 | 단위 | 가격 | 수량 | 관심품목 | |
Aloisine A, 1 mg | sc-202451 | 1 mg | $62.00 |
