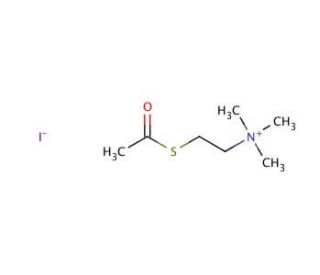
Acetylthiocholine iodide (CAS 1866-15-5)
Direktverknüpfungen
Acetylthiocholinjodid ist eine synthetische Verbindung, die als cholinerges Substrat fungiert und hauptsächlich in verschiedenen biochemischen Tests zur Untersuchung der Aktivität von Enzymen wie Acetylcholinesterase (AChE) und Butyrylcholinesterase (BChE) verwendet wird. Diese Enzyme spielen eine entscheidende Rolle bei der Hydrolyse von Cholinestern, und Acetylthiocholinjodid dient als spezifisches Substrat für die Quantifizierung ihrer enzymatischen Aktivität. Bei der Hydrolyse durch AChE oder BChE entsteht aus Acetylthiocholinjodid Thiocholin, das durch kolorimetrische oder elektrochemische Methoden nachgewiesen und quantifiziert werden kann, was die Bewertung der Enzymaktivität ermöglicht. Der Nutzen dieser Verbindung erstreckt sich auf die Untersuchung der Enzymkinetik, der Enzymhemmung und des Screenings von Inhibitoren, die die cholinergen Funktionen beeinflussen könnten, und trägt damit wesentlich zum Verständnis der Enzymmechanismen auf molekularer Ebene bei. Seine Rolle in der Forschung war ausschlaggebend für die Aufklärung der Dynamik der Neurotransmitterregulierung und der Enzymfunktionalität und ermöglichte Einblicke in die biochemischen Pfade, die der cholinergen Signalübertragung zugrunde liegen.
Acetylthiocholine iodide (CAS 1866-15-5) Literaturhinweise
- Kinetische und toxikologische Eigenschaften der Acetylcholinesterase aus den Kiemen von Austern (Crassostrea rhizophorae) und anderen aquatischen Arten. | Monserrat, JM., et al. 2002. Mar Environ Res. 54: 781-5. PMID: 12408650
- Histologie und Zytochemie der menschlichen Haut; die Verteilung der Cholinesterase in den Fingern des Embryos und des Erwachsenen. | BECKETT, EB., et al. 1956. J Physiol. 134: 202-6. PMID: 13377323
- Charakterisierung der Cholinesterase-Aktivität aus verschiedenen Geweben von Nil-Tilapia (Oreochromis niloticus). | Rodríguez-Fuentes, G. and Gold-Bouchot, G. 2004. Mar Environ Res. 58: 505-9. PMID: 15178074
- Cholinesterase-Inhibitoren aus Sargassum und Gracilaria gracilis: Meeresalgen, die in südindischen Küstengebieten (Hare Island, Golf von Mannar) vorkommen. | Natarajan, S., et al. 2009. Nat Prod Res. 23: 355-69. PMID: 19296376
- Cholinesterase hemmende Aktivitäten einiger Flavonoidderivate und ausgewählter Xanthone sowie deren molekulare Docking-Studien. | Khan, MT., et al. 2009. Chem Biol Interact. 181: 383-9. PMID: 19596285
- Kritische Bewertung von Acetylthiocholinjodid und Acetylthiocholinchlorid als Substrate für amperometrische Biosensoren auf der Basis von Acetylcholinesterase. | Bucur, MP., et al. 2013. Sensors (Basel). 13: 1603-13. PMID: 23353142
- Reversible und reproduzierbare In-vivo-Färbung von motorischen Endplatten mit Hilfe der Acetylthiocholin-Iodid-Methode. | Lindboe, CF. 1987. Acta Pathol Microbiol Immunol Scand A. 95: 245-9. PMID: 2442961
- Acetylcholinesterase der Erythrozytenmembran bei Diabetes mellitus Typ 1 (insulinabhängig). | Suhail, M. and Rizvi, SI. 1989. Biochem J. 259: 897-9. PMID: 2658981
- Mikroassay der Acetylcholinesterase-Aktivität in kleinen Portionen einzelner Mückenhomogenate. | Brogdon, WG. 1988. Comp Biochem Physiol C Comp Pharmacol Toxicol. 90: 145-50. PMID: 2904854
- Acetylcholinesterase. Kinetische Studien über den Mechanismus der Atropinhemmung. | Kato, G., et al. 1972. J Biol Chem. 247: 3186-9. PMID: 5027748
- Embryogenese bei Hymenolepis diminuta. V. Acetylcholinesterase in Embryonen. | Rybicka, K. 1967. Exp Parasitol. 20: 263-6. PMID: 6073592
- Verbesserte kolorimetrische Methode zur Bestimmung der Cholinesterase-Aktivität. | Venkataraman, BV., et al. 1993. Indian J Physiol Pharmacol. 37: 82-4. PMID: 8449554
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Acetylthiocholine iodide, 1 g | sc-208323 | 1 g | $37.00 | |||
Acetylthiocholine iodide, 5 g | sc-208323A | 5 g | $87.00 | |||
Acetylthiocholine iodide, 25 g | sc-208323B | 25 g | $369.00 | |||
Acetylthiocholine iodide, 100 g | sc-208323C | 100 g | $1176.00 | |||
Acetylthiocholine iodide, 250 g | sc-208323D | 250 g | $2710.00 |
