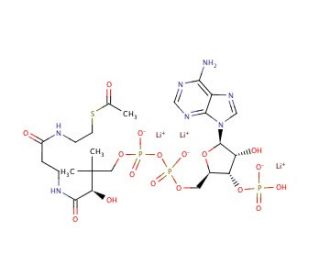
Molekülstruktur von Acetyl coenzyme A trilithium salt, CAS-Nummer: 32140-51-5
Acetyl coenzyme A trilithium salt (CAS 32140-51-5)
Produktreferenzen ansehen (1)
Alternative Namen:
Acetyl coenzyme A trilithium salt also known as Acetyl-S-CoA Li3; salt
Anwendungen:
Acetyl coenzyme A trilithium salt ist ein Cofaktor und Träger von Acylgruppen in enzymatischen Acetyltransferreaktionen
CAS Nummer:
32140-51-5
Molekulargewicht:
881
Summenformel:
C23H35N7O17P3S•3Li
Ausschließlich für Forschungszwecke. Nicht Geeignet für Verwendung in Diagnostik oder Therapie.
* Schauen Sie auf das Analysezertifikat (CoA), um die genauen Daten (inkl. Wassergehalt) Ihrer Produktionscharge (Lot) zu sehen.
Direktverknüpfungen
Bestellinformation
Publikationen
Beschreibung
Hintergrundinformationen
Sicherheitshinweis
SDS (SDB) & Analysenzertifikate
Acetyl-Coenzym A Trilithiumsalz ist ein Lithiumsalz eines essentiellen Cofaktors und Trägers von Acylgruppen in enzymatischen Acetyltransferreaktionen. Es entsteht entweder durch die oxidative Decarboxylierung von Pyruvat in den Mitochondrien, durch die Oxidation von langkettigen Fettsäuren oder durch den oxidativen Abbau bestimmter Aminosäuren. Acetyl-Coenzym A Trilithiumsalz ist ein Schlüsselvorläufer in der Lipidsynthese und die Quelle für alle Kohlenstoffatome in Fettsäuren. Acetyl-CoA ist ein positiver Regulator der Pyruvatcarboxylase und ein Vorläufer des Neurotransmitters Acetylcholin.
Acetyl coenzyme A trilithium salt (CAS 32140-51-5) Literaturhinweise
- Inhibitoren der Stickstoffmonoxid-Synthase dämpfen den durch den Nervenwachstumsfaktor vermittelten Anstieg der Cholin-Acetyltransferase-Expression in PC12-Zellen. | Kalisch, BE., et al. 2002. J Neurochem. 81: 624-35. PMID: 12065671
- Enzyme des Poly-(beta)-Hydroxybutyrat-Stoffwechsels in Sojabohnen- und Kichererbsen-Bacteroiden. | Kim, SA. and Copeland, L. 1996. Appl Environ Microbiol. 62: 4186-90. PMID: 16535445
- Formaldehyd-induzierte Histon-Modifikationen in vitro. | Lu, K., et al. 2008. Chem Res Toxicol. 21: 1586-93. PMID: 18656964
- Enzym-Nanopartikel-Biokonjugate mit zwei aufeinander folgenden Enzymen: Stöchiometrie und Aktivität von Malatdehydrogenase und Citratsynthase auf Au-Nanopartikeln. | Keighron, JD. and Keating, CD. 2010. Langmuir. 26: 18992-9000. PMID: 21114258
- Methoden für die Analyse von Acetyl-CoA-Synthase-Anwendungen in bakteriellen und archaeischen Systemen. | Grahame, DA. 2011. Methods Enzymol. 494: 189-217. PMID: 21402216
- LC-MS/MS-basierte Analyse von Coenzym A und kurzkettigen Acyl-Coenzym A-Thioestern. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- Die mitochondriale Sonde Methyltriphenylphosphonium (TPMP) hemmt das Krebszyklus-Enzym 2-Oxoglutarat-Dehydrogenase. | Elkalaf, M., et al. 2016. PLoS One. 11: e0161413. PMID: 27537184
- Kinetik der intrazellulären Elektronenerzeugung in Shewanella oneidensis MR-1. | Ishiki, K. and Shiigi, H. 2019. Anal Chem. 91: 14401-14406. PMID: 31631651
- In vitro N-terminale Acetylierung von bakteriell exprimierten Parvalbuminen durch N-terminale Acetyltransferasen aus Escherichia coli. | Lapteva, YS., et al. 2021. Appl Biochem Biotechnol. 193: 1365-1378. PMID: 32394317
- Hepatische N-Acetyltransferasen: Selektive Inaktivierung in vivo durch eine krebserregende N-Arylhydroxamsäure. | Smith, TJ. and Hanna, PE. 1988. Biochem Pharmacol. 37: 427-34. PMID: 3257389
- Veränderungen der Malat-Dehydrogenase-Isoenzyme während der Differenzierung von erythroiden Zellen aus dem Knochenmark von Kaninchen. | Setchenska, MS. and Arnstein, HR. 1979. Int J Biochem. 10: 817-21. PMID: 510663
- Verhinderung von Defekten des axonalen Transports und der Nervenleitgeschwindigkeit durch orale Verabreichung von Myo-Inositol oder eines Aldose-Reduktase-Hemmers bei Streptozotocin-diabetischen Ratten. | Mayer, JH. and Tomlinson, DR. 1983. Diabetologia. 25: 433-8. PMID: 6197336
- Vergleich der Entwicklungstoxizität und des Metabolismus von Nitrazepam bei Ratten und Mäusen. | Takeno, S., et al. 1993. Toxicol Appl Pharmacol. 121: 233-8. PMID: 8346540
- Schlüsselrolle von Acetyl-CoA im Zytoplasma von Nervenendigungen bei Störungen des Acetylcholinstoffwechsels im Gehirn. | Szutowicz, A., et al. 1997. Folia Neuropathol. 35: 241-3. PMID: 9833402
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Acetyl coenzyme A trilithium salt, 1 mg | sc-214465 | 1 mg | $69.00 | |||
Acetyl coenzyme A trilithium salt, 5 mg | sc-214465A | 5 mg | $119.00 | |||
Acetyl coenzyme A trilithium salt, 25 mg | sc-214465B | 25 mg | $389.00 | |||
Acetyl coenzyme A trilithium salt, 100 mg | sc-214465C | 100 mg | $1099.00 | |||
Acetyl coenzyme A trilithium salt, 250 mg | sc-214465D | 250 mg | $2599.00 | |||
Acetyl coenzyme A trilithium salt, 1 g | sc-214465E | 1 g | $6863.00 |
