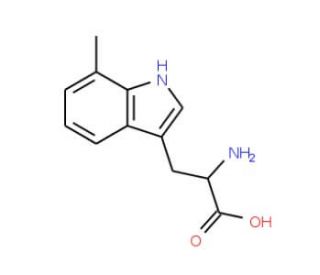
7-Methyl-DL-tryptophan (CAS 17332-70-6)
Produktreferenzen ansehen (1)
Direktverknüpfungen
7-Methyl-DL-Tryptophan, auch bekannt als 7-Me-DL-Trp, ist eine bedeutende Aminosäure, die in den Bereichen Biochemie und chemische Synthese weit verbreitet eingesetzt wird. Abgeleitet von der natürlichen Aminosäure Tryptophan besitzt diese Verbindung einzigartige Eigenschaften, die eine breite Anwendung finden. Im Bereich der wissenschaftlichen Forschung und Laborversuche spielt 7-Me-DL-Trp eine entscheidende Rolle. Es dient als wertvolles Substrat für Enzyme, als Marker für die Proteinsynthese und als Reagenz für die chemische Synthese. Seine Beteiligung erstreckt sich auf die Synthese von Peptiden, Proteinen, Antikörpern, Hormonen und anderen wichtigen Molekülen. Es hilft bei der Erforschung biochemischer Wege, was es ermöglicht, den Einfluss bestimmter Enzyme, Hormone und Moleküle auf zelluläre Prozesse zu untersuchen. Darüber hinaus zeigt diese Verbindung hemmende Eigenschaften gegenüber bestimmten Enzymen wie Tryptophanase, die an der Tryptophan-Abbau beteiligt sind.
7-Methyl-DL-tryptophan (CAS 17332-70-6) Literaturhinweise
- Hemmung der Beta-Amyloid-induzierten Neurotoxizität durch Imidazopyridoindole, die aus einer synthetischen kombinatorischen Bibliothek stammen. | Reixach, N., et al. 2000. J Struct Biol. 130: 247-58. PMID: 10940229
- Chemoenzymatische Synthese von prenylierten Indolderivaten unter Verwendung einer 4-Dimethylallyltryptophan-Synthase aus Aspergillus fumigatus. | Steffan, N., et al. 2007. Chembiochem. 8: 1298-307. PMID: 17577899
- Verwendung von 4-Methylindol oder 7-Methyl-DL-Tryptophan in einem System zur Selektion von Transformanten auf der Grundlage der rückkopplungsunempfindlichen Alpha-Untereinheit der Anthranilat-Synthase von Tabak (ASA2). | Barone, P. and Widholm, JM. 2008. Plant Cell Rep. 27: 509-17. PMID: 18060408
- Potenzial einer 7-Dimethylallyltryptophan-Synthase als Werkzeug für die Herstellung von prenylierten Indolderivaten. | Kremer, A. and Li, SM. 2008. Appl Microbiol Biotechnol. 79: 951-61. PMID: 18481055
- Substrat-Promiskuität der zyklischen Dipeptid-Prenyltransferasen aus Aspergillus fumigatus (Sektionszeichen). | Zou, H., et al. 2009. J Nat Prod. 72: 44-52. PMID: 19113967
- Plastidentransformation von Tabak unter Verwendung der rückkopplungsunempfindlichen Anthranilat-Synthase-[alpha]-Untereinheit von Tabak (ASA2) als neuer selektierbarer Marker. | Barone, P., et al. 2009. J Exp Bot. 60: 3195-202. PMID: 19553372
- Biochemische Charakterisierung von Indol-Prenyltransferasen: Auffüllen der letzten Lücke der Prenylierungspositionen durch eine 5-Dimethylallyltryptophan-Synthase aus Aspergillus clavatus. | Yu, X., et al. 2012. J Biol Chem. 287: 1371-80. PMID: 22123822
- Die Tyrosin-O-Prenyltransferase SirD katalysiert S-, C- und N-Prenylierungen an Tyrosin- und Tryptophan-Derivaten. | Rudolf, JD. and Poulter, CD. 2013. ACS Chem Biol. 8: 2707-14. PMID: 24083562
- Tryptophan- und Indolanalog-vermittelte Plastidtransformation. | Barone, P., et al. 2014. Methods Mol Biol. 1132: 187-203. PMID: 24599854
- Eine 7-Dimethylallyl-Tryptophan-Synthase aus einem Pilz (Neosartorya sp.): biochemische Charakterisierung und strukturelle Einblicke in die regioselektive Prenylierung. | Miyamoto, K., et al. 2014. Bioorg Med Chem. 22: 2517-28. PMID: 24657051
- Strukturelle Grundlage für die Produktion von β-Carbolin-Alkaloiden durch das mikrobielle homodimere Enzym McbB. | Mori, T., et al. 2015. Chem Biol. 22: 898-906. PMID: 26120001
- Charakterisierung von 6-DMATSMo aus Micromonospora olivasterospora zur Identifizierung der Divergenz in der Enantioselektivität, Regioselektivität und Mehrfachprenylierung von Tryptophan-Prenyltransferasen. | Winkelblech, J., et al. 2016. Org Biomol Chem. 14: 9883-9895. PMID: 27714299
- Die effiziente Methylierung von C2 in L-Tryptophan durch die Cobalamin-abhängige radikale S-Adenosylmethionin-Methylase TsrM erfordert ein unmodifiziertes N1-Amin. | Blaszczyk, AJ., et al. 2017. J Biol Chem. 292: 15456-15467. PMID: 28747433
- Enantioseparation von Tryptophan und seinen unnatürlichen Derivaten durch Nano-LC auf CSP-Teicoplanin-Silikatbasis. | D'Orazio, G., et al. 2019. Electrophoresis. 40: 1966-1971. PMID: 30725477
- Wirkung von Tryptophan-Analoga auf die Derepression des Tryptophan-Operons von Escherichia coli durch Indol-3-propionsäure. | Pauley, RJ., et al. 1978. J Bacteriol. 136: 219-26. PMID: 361689
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
7-Methyl-DL-tryptophan, 100 mg | sc-281501 | 100 mg | $143.00 | |||
7-Methyl-DL-tryptophan, 250 mg | sc-281501A | 250 mg | $296.00 |
