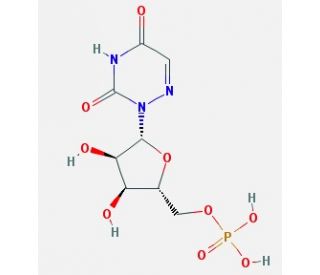
6-Azauridine-5′-monophosphate (CAS 2018-19-1)
Produktreferenzen ansehen (1)
Direktverknüpfungen
6-Aza Uridin 5'-Monophosphat (6-AU5P) hat eine immense Bedeutung in den Bereichen Biochemie und Molekularbiologie. Dieser modifizierte Nukleosid spielt eine entscheidende Rolle bei der Synthese verschiedener Moleküle und findet weitreichende Anwendungen in der wissenschaftlichen Forschung. Im wissenschaftlichen Forschungslandschaft findet 6-Aza Uridin 5'-Monophosphat eine umfangreiche Nutzung. Seine Verwendung reicht von der Synthese modifizierter Nukleoside und Nukleotide, die die Untersuchung von DNA und RNA ermöglichen. Darüber hinaus dient es als Schlüsselkomponente bei der Synthese modifizierter Proteine, was die Untersuchung von Protein-Protein-Interaktionen ermöglicht. Außerdem spielt 6-Aza Uridin 5'-Monophosphat eine wichtige Rolle bei der Synthese modifizierter Kohlenhydrate, was die Untersuchung von Kohlenhydrat-Protein-Interaktionen ermöglicht. Funktionell fungiert 6-Aza Uridin 5'-Monophosphat als Inhibitor der DNA- und RNA-Synthese. Sein Mechanismus beinhaltet die Bindung an die aktive Site des Enzyms Ribonukleotidreduktase, das für die Konvertierung von Ribonukleotiden in Deoxyribonukleotide verantwortlich ist. Durch die Bindung an dieses Enzym behindert 6-Aza Uridin 5'-Monophosphat den Konvertierungsprozess und verhindert somit die DNA- und RNA-Synthese.
6-Azauridine-5′-monophosphate (CAS 2018-19-1) Literaturhinweise
- 6-Azauracil-resistenten Varianten von kultivierten Pflanzenzellen fehlt die Uracil-Phosphoribosyltransferase-Aktivität. | Jones, GE. 1984. Plant Physiol. 75: 161-5. PMID: 16663563
- Entwicklung von Inhibitoren der Orotidinmonophosphat-Decarboxylase unter Verwendung von bioisosterischem Ersatz und Bestimmung der Hemmungskinetik. | Poduch, E., et al. 2006. J Med Chem. 49: 4937-45. PMID: 16884305
- Eine Untersuchung des Verhältnisses zwischen der Größe der Schleife des aktiven Zentrums und den thermodynamischen Aktivierungsparametern für Orotidin-5'-monophosphat-Decarboxylase aus mesophilen und thermophilen Organismen. | Toth, K., et al. 2009. Biochemistry. 48: 8006-13. PMID: 19618917
- Kristallisation von Hefe-Orotidin-5'-monophosphat-Decarboxylase, komplexiert mit 1-(5'-Phospho-beta-D-ribofuranosyl)-Barbitursäure. | Bell, JB., et al. 1991. Proteins. 9: 143-51. PMID: 2008434
- Reinigung und Charakterisierung von Orotidin-5'-Monophosphat-Decarboxylase aus Hefe, die aus dem Plasmid PGU2 überexprimiert wird. | Bell, JB. and Jones, ME. 1991. J Biol Chem. 266: 12662-7. PMID: 2061334
- Protonentransfer von C-6 von Uridin-5'-monophosphat, katalysiert durch Orotidin-5'-monophosphat-Decarboxylase: Bildung und Stabilität eines Vinylcarbanion-Zwischenprodukts und die Wirkung eines 5-Fluor-Substituenten. | Tsang, WY., et al. 2012. J Am Chem Soc. 134: 14580-94. PMID: 22812629
- Atomare Auflösungsstruktur des Orotidin-5'-Monophosphat-Decarboxylase-Produktkomplexes in Kombination mit Oberflächenplasmonenresonanzanalyse: Auswirkungen auf den katalytischen Mechanismus. | Fujihashi, M., et al. 2013. J Biol Chem. 288: 9011-6. PMID: 23395822
- Architektur der Enzyme: Aufbrechen des katalytischen Käfigs, der die Orotidin-5'-Monophosphat-Decarboxylase für die Katalyse aktiviert. | Reyes, AC., et al. 2018. J Am Chem Soc. 140: 17580-17590. PMID: 30475611
- Orotidin-5'-Monophosphat-Decarboxylase: Die Funktionsweise von Active Site Chains innerhalb und zwischen den Proteinuntereinheiten. | Brandão, TAS. and Richard, JP. 2020. Biochemistry. 59: 2032-2040. PMID: 32374983
- Untersuchung der kinetischen und physikalischen Eigenschaften der Orotidin-5'-monophosphat-Decarboxylase-Domäne der UMP-Synthase der Maus, die in Saccharomyces cerevisiae produziert wird. | Langdon, SD. and Jones, ME. 1987. J Biol Chem. 262: 13359-65. PMID: 3308878
- Die Reinigung und vorläufige Charakterisierung der UMP-Synthase aus der menschlichen Plazenta. | Livingstone, LR. and Jones, ME. 1987. J Biol Chem. 262: 15726-33. PMID: 3680222
- H NMR-Studie über die Konformation des Ribosephosphatanteils von 6-Azauridin-5'-monophosphat - ein Nukleotid mit einer ungewöhnlichen Konformation. | Hruska, FE., et al. 1973. FEBS Lett. 31: 153-5. PMID: 4709996
- In-vivo-Synthese von 6-Azauridin-5'-Triphosphat und Einbau von 6-Azauridin in RNA keimender Weizen-Embryonalachsen. | Rodaway, S. and Marcus, A. 1980. J Biol Chem. 255: 8402-4. PMID: 6157685
- Erhöhung des intrazellulären 5-Phosphoribosyl-1-Pyrophosphat-Spiegels als Hauptfaktor bei der 6-Azauridin-induzierten Stimulierung der Carbamoylphosphat-Synthese in Milzschnitten der Maus. | Tatibana, M., et al. 1982. Eur J Biochem. 128: 631-6. PMID: 6185335
- Isolierung und teilweise Charakterisierung einer 5'-Nukleotidase, die spezifisch für Orotidin-5'-monophosphat ist. | El Kouni, MH. and Cha, S. 1982. Proc Natl Acad Sci U S A. 79: 1037-41. PMID: 6280163
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
6-Azauridine-5′-monophosphate, 10 mg (Out of Stock: Availability 9/5/25) | sc-291171B | 10 mg | $151.00 | |||
6-Azauridine-5′-monophosphate, 25 mg | sc-291171C | 25 mg | $286.00 | |||
6-Azauridine-5′-monophosphate, 50 mg | sc-291171 | 50 mg | $473.00 | |||
6-Azauridine-5′-monophosphate, 100 mg | sc-291171A | 100 mg | $837.00 | |||
6-Azauridine-5′-monophosphate, 250 mg | sc-291171D | 250 mg | $1753.00 |
