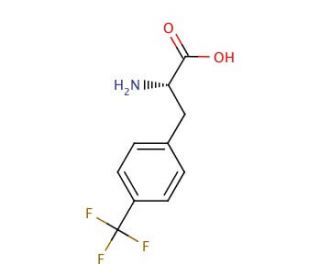
4-(Trifluoromethyl)-L-phenylalanine (CAS 114926-38-4)
Direktverknüpfungen
4-(Trifluormethyl)-L-phenylalanin ist eine Verbindung, die in der Peptidsynthese als nicht natürliche Aminosäure fungiert. Sie wird verwendet, um eine Trifluormethylgruppe in Peptide einzuführen, die deren physikochemische Eigenschaften und biologische Aktivität verändern kann. Der Wirkungsmechanismus von 4-(Trifluormethyl)-L-phenylalanin besteht darin, dass es während der Festphasen-Peptidsynthese in die Peptidsequenz eingebaut wird. Diese nicht natürliche Aminosäure kann die Konformation und Stabilität des Peptids sowie seine Wechselwirkungen mit biologischen Zielstrukturen beeinflussen. Auf molekularer Ebene kann 4-(Trifluormethyl)-L-phenylalanin die Bindungsaffinität, die enzymatische Aktivität oder die zelluläre Aufnahme des Peptids beeinflussen, je nach spezifischer Sequenz und Kontext. Seine einzigartige chemische Struktur ermöglicht die Erforschung von Struktur-Aktivitäts-Beziehungen und die Entwicklung von peptidbasierten Sonden oder potenziell biologisch aktiven Verbindungen.
4-(Trifluoromethyl)-L-phenylalanine (CAS 114926-38-4) Literaturhinweise
- Die Einführung von Fluoratomen oder Trifluormethylgruppen in kurze kationische Peptide erhöht deren antimikrobielle Aktivität. | Giménez, D., et al. 2006. Bioorg Med Chem. 14: 6971-8. PMID: 16809042
- Glykosaminoglykanbindung und nicht-endozytäre Membrantranslokation von zellpermeablem Octaarginin, überwacht durch Echtzeit-NMR-Spektroskopie in der Zelle. | Takechi-Haraya, Y., et al. 2017. Pharmaceuticals (Basel). 10: PMID: 28420127
- Aktuelles Verständnis der physikalisch-chemischen Mechanismen für die Zellmembranpenetration von Arginin-reichen zelldurchdringenden Peptiden: Die Rolle von Glykosaminoglykan-Interaktionen. | Takechi-Haraya, Y. and Saito, H. 2018. Curr Protein Pept Sci. 19: 623-630. PMID: 29332576
- Lösungs-NMR zur Quantifizierung der Mobilität in Membranen: Diffusion, Protrusion und Wirkstofftransportprozesse. | Okamura, E. 2019. Chem Pharm Bull (Tokyo). 67: 308-315. PMID: 30930433
- Design und kombinatorische Entwicklung von Shield-1 Peptidmimetika, die an destabilisiertes FKBP12 binden. | Madsen, D., et al. 2020. ACS Comb Sci. 22: 156-164. PMID: 32027120
- Modulierung der co-translationalen Proteinfaltung durch rationales Design und Ribosomen-Engineering. | Ahn, M., et al. 2022. Nat Commun. 13: 4243. PMID: 35869078
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-(Trifluoromethyl)-L-phenylalanine, 1 g | sc-226438 | 1 g | $206.00 |
