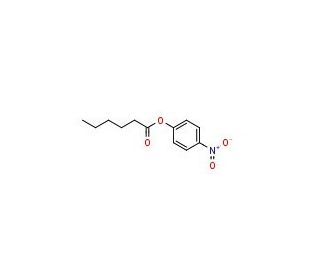
4-Nitrophenyl Hexanoate (CAS 956-75-2)
Direktverknüpfungen
4-Nitrophenylhexanoat ist ein interessanter Stoff in der organischen Chemie und Enzymologie aufgrund seiner Fähigkeit, als Substrat für Esterasen und Lipasen zu wirken, Enzyme, die Esterbindungen hydrolysieren. In Kinetikstudien wird dieses Ester häufig verwendet, um die Aktivität und Spezifität dieser Enzyme zu bewerten und Einblicke in ihre Wirkmechanismen zu erhalten. Dies hat Auswirkungen auf das Verständnis der Lipidmetabolismus und die Synthese von Biodiesel, wo solche Enzyme eingesetzt werden, um die Transesterifikation von Triglyceriden zu katalysieren. In der organischen Synthese kann 4-Nitrophenylhexanoat in der Synthese komplexer organischer Moleküle eingesetzt werden, als Esterifizierungsmittel, das Hexanoatgruppen einführt. Darüber hinaus ist bekannt, dass das Nitrophenylmoiety des Moleküls bei enzymatischer Spaltung ein gefärbtes Produkt freisetzt, was nützlich ist in spektrophotometrischen Assays, die Enzymaktivität und kinetische Parameter messen.
4-Nitrophenyl Hexanoate (CAS 956-75-2) Literaturhinweise
- Reaktionen innerhalb von Assoziationskomplexen: die Reaktion von Imidazol mit substituierten Phenylacetaten in Gegenwart von Detergenzien in wässriger Lösung. | Pirinccioglu, N., et al. 2000. J Org Chem. 65: 2537-43. PMID: 10789468
- Ein Substrat-induzierter Wechsel im Reaktionsmechanismus einer thermophilen Esterase: kinetische Beweise und strukturelle Grundlage. | De Simone, G., et al. 2004. J Biol Chem. 279: 6815-23. PMID: 14617621
- Katalyse durch hydrophobisch modifizierte Poly(propylenimin)-Dendrimere mit quaternärer Ammonium- und tertiärer Aminfunktionalität. | Murugan, E., et al. 2004. Langmuir. 20: 8307-12. PMID: 15350107
- Durch Gallensalz stimulierte Lipase und Mucine aus der Milch von 'sekretorischen' Müttern hemmen die Bindung von Norwalk-Virus-Kapsiden an ihre Kohlenhydrat-Liganden. | Ruvoën-Clouet, N., et al. 2006. Biochem J. 393: 627-34. PMID: 16266293
- Expression und Charakterisierung einer neuen enantioselektiven Lipase aus Aspergillus fumigatus. | Shangguan, JJ., et al. 2012. Appl Biochem Biotechnol. 168: 1820-33. PMID: 23054817
- Experimentelle und theoretische Untersuchung des Mechanismus der Hydrolyse von substituierten Phenylhexanoaten, katalysiert durch Globin in Gegenwart eines Tensids. | Ercan, S., et al. 2014. J Mol Model. 20: 2096. PMID: 24562853
- Reinigung und Charakterisierung der Esterase 2B der Hausmaus, Mus musculus. | Lexow, U., et al. 1980. Eur J Biochem. 107: 123-30. PMID: 6772441
- Reinigung und Charakterisierung der Esterase 1F, der Albumin-Esterase der Hausmaus (Mus musculus). | Otto, J., et al. 1981. Eur J Biochem. 116: 285-91. PMID: 6788549
- Reinigung und Charakterisierung der Esterase 6A, einer trimeren Esterase der Hausmaus (Mus musculus). | Oehm, HC., et al. 1982. Eur J Biochem. 129: 157-63. PMID: 7160378
- Assoziation von Gallensalz-abhängiger Lipase mit Membranen menschlicher Pankreas-Mikrosomen. | Bruneau, N., et al. 1995. Eur J Biochem. 233: 209-18. PMID: 7588748
- Eine Untersuchung der Aktivitäten und Paraoxon-Empfindlichkeiten hepatischer Aliesterasen in Beta-Naphthoflavon-behandelten Ratten. | Watson, AM., et al. 1994. Toxicol Lett. 71: 217-25. PMID: 8160210
- Esterase-30 (ES-30) der Hausmaus: biochemische Charakterisierung und Genetik eines neuen Carboxylesterase-Isozyms, das mit Cluster-2-Loci auf Chromosom 8 verbunden ist. | Ronai, A., et al. 1993. Biochem Genet. 31: 279-94. PMID: 8274135
- Untersuchung von zwei glykosylierten Formen der gallensalzabhängigen Lipase im menschlichen Pankreassaft. | Mas, E., et al. 1997. Eur J Biochem. 243: 299-305. PMID: 9030752
- Die Assoziation von gallensalzabhängiger Lipase mit Membranen menschlicher Pankreasmikrosomen unterliegt der Kontrolle von ATP und Phosphorylierung. | Pasqualini, E., et al. 1997. Biochem J. 327 (Pt 2): 527-35. PMID: 9359426
- Gallensalzabhängige Lipaseaktivität der Bauchspeicheldrüse im Serum von normolipidämischen Patienten. | Caillol, N., et al. 1997. Lipids. 32: 1147-53. PMID: 9397399
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
4-Nitrophenyl Hexanoate, 1 g | sc-486520 | 1 g | $162.00 |
